-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
遺伝子の変化や変異の種類によって、身体に様々な影響を与えることがあります。時には、遺伝子の特定の変異によって、タンパク質が機能しなくなったり、全く合成されなくなったりすることがあります。嚢胞性線維症は、嚢胞性線維症膜貫通コンダクタンスレギュレータ(CFTR)をコードする遺伝子の変異によって引き起こされます。このタンパク質は、上皮組織におけるイオンや水分の分泌・吸収を調節する役割を担っています。以前は、遺伝性疾患である嚢胞性線維症(CF)について紹介しましたが、今回は、CFTR遺伝子とその主要な6種類の変異、そしてCFTRマウスモデルの研究への応用について解説します。
嚢胞性線維症の遺伝子変異
嚢胞性線維症(CF)は、CFTR遺伝子の変異によって引き起こされる常染色体劣性遺伝性の疾患であり、主に気道上皮細胞、小腸、膵臓、肝臓、唾液腺、生殖管などの上皮組織の正常な機能に影響を及ぼします。
CFTR遺伝子は、7番染色体長腕(7q31.2)に位置し、全長250kb、1480アミノ酸、27エキソン、26イントロンを有しています。CFTR遺伝子は、12個の膜貫通ドメイン、2個のヌクレオチド結合ドメイン(NBD1/2)、調節(R)ドメインからなる嚢胞性線維症膜貫通コンダクタンスレギュレータ(CFTR)タンパク質をコードしています。RドメインにはプロテインキナーゼA(PKA)とプロテインキナーゼC(PKC)が共有するリン酸化部エキソン、プロテインキナーゼがリン酸化されると、CFTRのクロライドチャネルが開かれます。
CFTRタンパク質は、ATP-binding cassette(ABC) トランスポーターファミリーの一員であり、真核生物やバクテリアにおいて、栄養素の取り込み、基質の輸出、細胞間情報伝達の仲介などに関与しています。粘膜腺に発現し、体液や電解質の分泌を促進し、粘膜腺から気道にムチン、複合糖質、抗菌剤を分泌して粘膜繊毛クリアランスと自己防衛を促進します。
CFTRの変異は、クロライドチャネルの異常な活性化を引き起こし、細胞による塩分イオンと水分の取り込みの調節に影響を及ぼします。その結果、チャネル内の粘液が粘性を帯び、膵臓や呼吸器などの臓器で塞栓を引き起こします。その上、汗管内の塩化ナトリウムが再吸収されなくなり、非常に塩辛い汗をかくことになります。
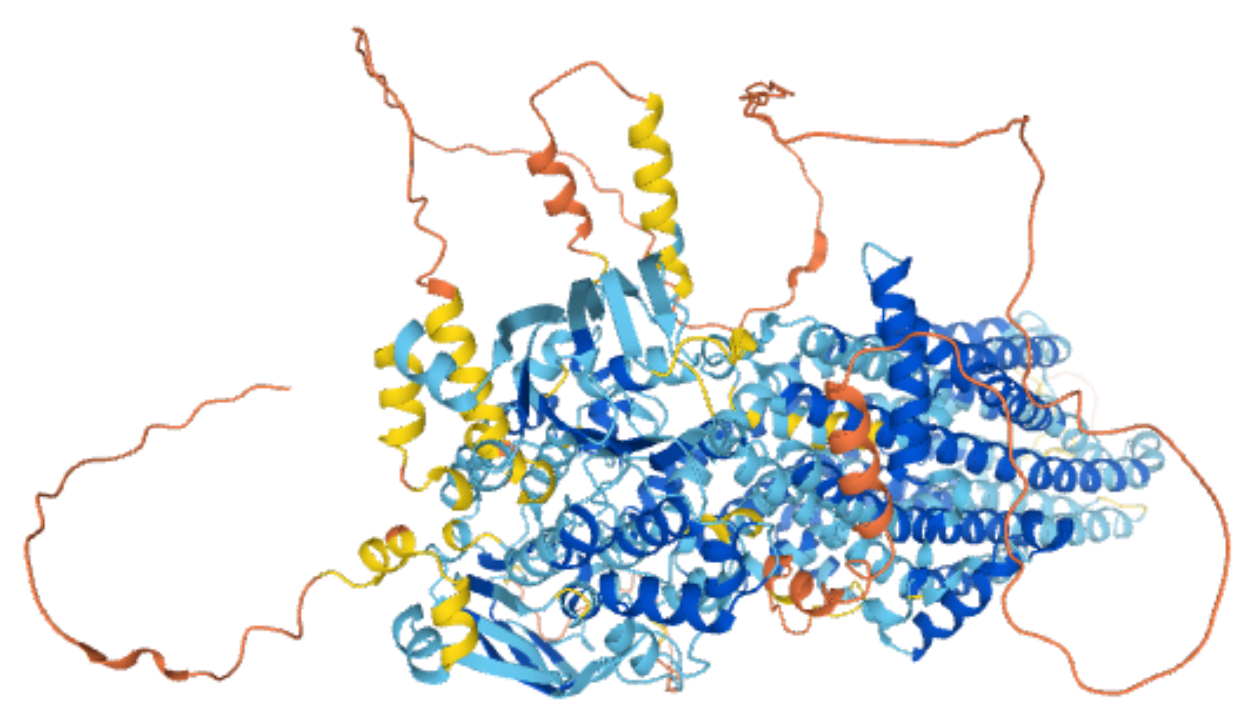
図1. CFTRタンパク質の構造予測
CFTRの活性化は環状アデノシン一リン酸(cAMP)を介して行われ、そのヌクレオチド結合ドメイン(NBD)はアデノシン三リン酸(ATP)に結合しますが、一部の研究ではcAMPに依存せずに実現されることも示唆されています。
CFTRは、イオンチャネルの制御において重要な役割を担っており、水分子の輸送を伴う細胞内の塩化物イオンの膜を介した移動を仲介しています。CFTRがクロライドチャネルを制御する過程は以下の通りです。
(1)cAMPのレベルが上昇すると、Rドメインのセリンがリン酸化されます。
(2)セリンのリン酸化により、NBDドメインへのATP結合が促進されます。
(3)NBD1末端のリン酸がせん断されると、CFTRの全体構造が変化し、イオンチャネルが開口します。
(4)NBDB2に結合したATPが加水分解されると、CFTRの構造は再び変化し、チャネルは閉じられます。
CFTRは、塩化物イオンの流出を媒介することに加えて、以下のことが可能です。
(1)腎外髄質カリウムチャネル(ROMK2)を介して、CFTRは細胞内のNBD1および調節(R)ドメインと相互作用し、K(+)の輸送を調節します。
(2)CFTRは、プリン作動性受容体 (PY2R) に ATP が結合することで、外向き整流性Cl(-)チャネル(ORCC)の活性を調節することができます。
(3)CFTRは ENaCタンパクを阻害し、細胞内への Na(+)輸送を制御することができます。
正常なCFTR充足細胞では、機能的なCFTRタンパク質は細胞膜に正しく輸送されています。現在までに2,000以上のCFTRの変異が同定されており、6つのカテゴリーに分類されています。
クラスI変異 (G543X)
クラスIの変異は、CFTRのタンパク質合成の欠如をもたらします。
クラスII変異(△F508)
クラスII変異は最も一般的なCFTRの変異です。この変異は、エキソン10における3塩基対の欠失により、タンパク質の508位のフェニルアラニン欠失を引き起こしたことに起因します。CFTRに△F508変異遺伝子を持つCF患者は、全体の88.5%を占めています。この変異により、CFTRの成熟が阻害され、小胞体(ER)においてミスフォールドしたタンパク質が分解されます。
クラスIII変異(G551D)
クラスIIIの変異は、CFTRの制御に影響を与え、CFTRチャネルの機能を低下させます。
クラスIV変異(R117H)
クラスIVの変異は、Cl(-)コンダクタンスの減少を引き起こす可能性があります。
クラスV変異(3849+10kb C-T)
クラスVの変異は、機能的なCFTRタンパクの合成を減少させます。
クラスVI変異(Q1412X)
クラスVI変異は、細胞膜におけるCFTRの安定性を低下させます。
CF研究におけるマウスモデルの活用
CFTRのアミノ酸配列の相同性は、ヒトとマウスで78%です。最初のCFTRノックアウトマウスCFTRtm1UNCは、CFTRコード配列のエキソン10に停止コドンを挿入することにより作製され、S489X変異と呼ばれ、重度の腸管合併症を有しています。
CFTRノックアウトマウスは、CFTRtm1CAM、CFTRtm1HSC、CFTRtm1BAY、CFTRtm3BAYモデルなど、様々な遺伝子背景を持つより多くのモデルが存在します。これらのマウス株はいずれも野生型CFTRのmRNAが検出されず、CFTRtm1CAMは重度の膵管閉塞を伴う腸の表現型を示し、CFTRtm1HSC、CFTRtm1BAY、CFTRtm3BAYはいずれも重度の腸の合併症を有しています。
CFのノックアウトモデル以外にも、ΔF508変異を持つマウス(CFTRtm1EUR、CFTRtm1KTH、CFTRtm2CAM)、G480C変異を持つCFTRtm2HGU、G551D変異を持つCFTRtm1G551Dなど、様々なノックインミュータントも開発されています。このうち、CFTRtm1EURモデルは、腸の異常表現型が非致死的ではあるものの、膵臓と肝臓には異常がなく、CFTRtm1KTHモデルの精子は異常表現型ではあるものの、胆嚢と膵臓には異常がなく、ノックアウトマウスよりも長く生存することができました。
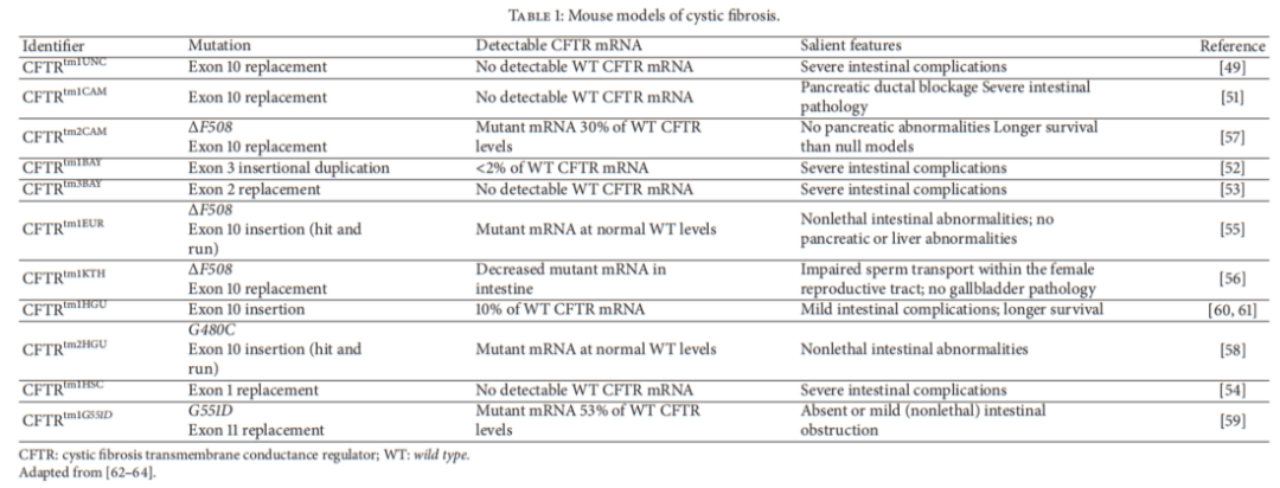
図2. 嚢胞性線維症のマウスモデル
嚢胞性線維症の研究において、ノックアウトマウスやノックインマウスは、作製が容易で、飼育期間が短く、飼育コストが低いという利点がありますが、種によってモデルの病勢が一定しないため、やはり一定の限界が存在します。例えば、上記のマウスモデルでは、患者と同様の重篤な腸閉塞、成長阻害、嗅覚電気生理学的異常などを示すことができますが、肺の自然感染は見られませんでした。そして、ほとんどの実験結果は、マウスの膵臓、肝臓、精管に軽度の合併症が発生しただけであり、患者の症状とは大きく異なっていました。
これらの違いの原因は、マウスではCFTRの発現が低〜中程度でも十分なイオン輸送能が得られ、病気が重篤化しないためと考えられます。また、マウスでは、CFTRとは別のシグナル伝達経路を持つ第2のCl(-)チャネルの上皮発現が、CFTRの機能不全を補っている可能性があります。
そこで、一部の研究者は、ヒトCFTR遺伝子を含む細菌人工染色体(BAC)をCFTRノックアウトマウスに移植し、この制限を克服しようとしました。その結果、ヒトCFTRを発現するマウスの腸管や呼吸器の異常表現型は、患者のそれと類似していることが確認されました。また、CFTR遺伝子はマウスとヒトの間で一定程度保存されていることが証明されました。
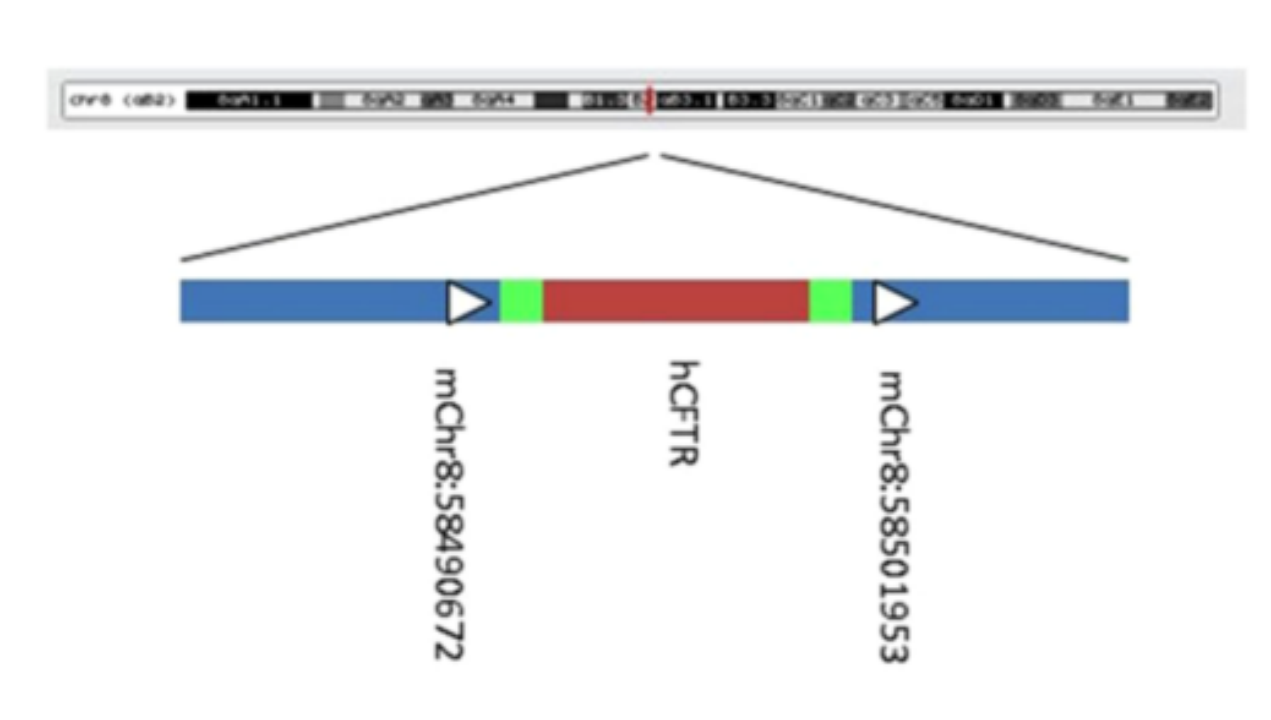
図3. ヒト化マウスの構築
非コード領域の研究
CFTRの5'-非翻訳領域(5'-UTR)中の緑色の枠で囲んだ部分をルシフェラーゼで標識した5'-UTRに置き換え、ルシフェラーゼの蛍光でその配列の機能を判定しました。その結果、上流のAUGコドン(uAUG)をUUGコドン(uUUG)に変異させ、下流のステムの配列を変異させた場合、変異配列のルシフェラーゼ発現効率は野生型CFTRの5'UTR配列のそれよりも著しく高くなることが判明しました。また、トップステムの配列を変異させた場合にも同様の結果が得られました。以上のことから、CFTRの5'UTRの治療的価値の可能性が示唆されました。
また、CFTR mRNA上には多数のmiRNA結合部位が存在することが報告されています。miR-145-5pはCFTRなどと相互作用してCFTRの合成を阻害し、miR-145-5pを標的としたペプチド核酸(PNA)R8-PNA-a145はmiR-145-5pの発現抑制とCFTR mRNAのアップレギュレーションを実現できると考えられました。以上のことから、CFTRの3'UTRの治療的価値の可能性が示唆されました。
サイヤジェンCFTRマウスによる研究加速化への支援
この研究テーマにご興味のある方は、ノックアウトカタログモデルをご覧ください。今回ご紹介したCFTR遺伝子ノックアウトマウスやコンディショナルノックアウトマウスは、最短で7~9週間でお届けすることが可能です !また、価格マッチング保証により、お客様の研究に最も適したコストパフォーマンスの高い実験用マウスを簡単に入手できます!
他にもお探しでしょうか?他にもたくさんの遺伝子改変マウスをご用意しております。ご相談やご注文は、メール([email protected])にて承っております。
参考文献:
[1] Lavelle GM, White MM, Browne N, McElvaney NG, Reeves EP. Animal Models of Cystic Fibrosis Pathology: Phenotypic Parallels and Divergences. Biomed Res Int. 2016;2016:5258727.doi:10.1155/2016/5258727. Epub 2016 Jun 1.
[2] Rosen BH, Chanson M, Gawenis LR, Liu J, Sofoluwe A, Zoso A, Engelhardt JF. Animal and model systems for studying cystic fibrosis. J Cyst Fibros. 2018 Mar;17(2S):S28-S34. doi: 10.1016/j.jcf.2017.09.001. Epub 2017 Sep 19.
[3] Gawenis LR, Hodges CA, McHugh DR, Valerio DM, Miron A, Cotton CU, Liu J, Walker NM, Strubberg AM, Gillen AE, Mutolo MJ, Kotzamanis G, Bosch J, Harris A, Drumm ML, Clarke LL. A BAC Transgene Expressing Human CFTR under Control of Its Regulatory Elements Rescues Cftr Knockout Mice. Sci Rep. 2019 Aug 14;9(1):11828. doi: 10.1038/s41598-019-48105-4.
[4] Fabbri E, Tamanini A, Jakova T, Gasparello J, Manicardi A, Corradini R, Sabbioni G, Finotti A, Borgatti M, Lampronti I, Munari S, Dechecchi MC, Cabrini G, Gambari R. A Peptide Nucleic Acid against MicroRNA miR-145-5p Enhances the Expression of the Cystic Fibrosis Transmembrane Conductance Regulator (CFTR) in Calu-3 Cells. Molecules. 2017 Dec 29;23(1):71. doi: 10.3390/molecules23010071.513.html
