-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
目のケアというと、まず近視を思い浮かべる人が多いのですが、目にも何らかの合併症となることを見落としがちです。高血糖や高血圧を患うと、遠からず糖尿病網膜症(DR)が進行している可能性があります。
一、DRの高い有病率
糖尿病網膜症(DR)は、糖尿病患者によく見られる微小血管の合併症です。米国では、2型糖尿病患者の40%、1型糖尿病患者の86%がDR患者であるといわれています。中国人を対象とした横断研究では、中国の農村部には30歳以上の糖尿病患者が2110万人もおり、そのうち約920万人がDRであることが明らかになっています。また、英国、オーストラリア、アジアの他の国々のコホート研究でも、DRの有病率は20%~50%と報告されています。
二、DRの臨床的分類
糖尿病網膜症は、その発症段階と重症度により、非増殖性糖尿病網膜症(NPDR)と増殖性糖尿病網膜症(PDR)の2つに分類されます。米国のウィスコンシン糖尿病疫学研究(WESDR)の10年間のコホート研究では、糖尿病と診断された患者の17%が視力を脅かす重度のPDRを発症しています。また、別の25年間のコホート研究では、時間の経過とともに1型糖尿病患者の97%がDRを発症し、そのうち43%がPDRを発症したことが示されています。PDRは、網膜の病的血管新生と線維血管増殖を特徴とするDRの進行期です。さらに合併症として硝子体出血(VH)や牽引性網膜剥離(TRD)を発症すると、重度の視力障害や失明を引き起こすこともあります。
三、DRおよび関連疾患の動物モデル
動物モデルは、疾患の発症メカニズムを理解するための重要な研究ツールです。また、適切な動物モデルは、臨床薬効評価にも大きく貢献します。
1. DR動物モデル
DR動物モデルは、高血糖の自然発症、手術、遺伝子編集など様々なモデル化のアプローチによって確立することができます。
遺伝子改変マウス
DRの遺伝子モデルマウスには、主にAkita、非肥満性糖尿病(NOD)、db/db、Kimba、Akimbaの5種類があり、遺伝様式、病因、病態、疾患進行などが異なります。
- Akitaマウスは、1型糖尿病のモデルマウスです。その構築原理は、主にインスリン遺伝子Ins2の変異により、インスリンタンパク質の構造変化が起こり、最終的に細胞死を引き起こすというものです。このモデルは、血管透過性の亢進、周皮細胞の喪失、新生血管の形成によって特徴づけることができます。したがって、Akitaマウスは、DRの初期進行の研究や神経保護薬の薬効評価に適しています[1]。
- NODマウスは、1型糖尿病のモデルマウスです。マウスは12週齢で高血糖を自然発症し、4週間の血糖上昇後、周皮細胞、内皮細胞、網膜神経節細胞(RGC)のアポトーシスが始まり、網膜毛細血管の基底膜が厚くなり、4ヶ月齢頃には大血管の収縮と変性、微小血管の異常が検出できるようになります。
- db/dbマウスは、自然発症2型糖尿病のモデルマウスです。そのレプチン受容体に変異が生じ、生後4〜8週でマウスの肥満と高血糖が起こり、6週後にはRGC数の減少と中心網膜の厚みが増し、15ヵ月後には血液網膜関門(BRB)の破綻、周皮細胞の消失、RGCのアポトーシス、グリア細胞の活性化が起こります。
- Kimbaマウスは、非糖尿病性の増殖性網膜症モデルです。Akimbaマウスは、ホモ接合体KimbaマウスとAkitaマウスとの交配により、作製されました。
- KimbaマウスとAkitaマウスの両方の特徴を持ち[2]、主に周皮細胞や血管の消失、網膜新生血管、びまん性血管漏出などが見られます。病気の進行に伴い、網膜の厚みの減少や持続的な網膜浮腫、さらには網膜剥離がマウスモデルで観察されることがあります。
図注:希少疾患データセンター(RDDC)では、ユーザは興味のある疾患を入力するだけで、関連する動物モデルを見ることができます。
誘発動物モデル
- STZ誘発モデル
薬物誘発モデルは、モデル化の容易さと病態変化を正確に再現できることから、DRの動物モデルとしてよく用いられるようになり、主にストレプトゾシン(STZ)とアロキサン(AXL)によって誘発される糖尿病モデルがあります。STZは糖尿病誘発に最もよく用いられる薬物であり、その作用機序は主に膵β細胞を破壊することにより高血糖を引き起こすことにあります。STZ誘発糖尿病ラットでは、2〜4週齢でBRBの破壊が起こり、4〜6週齢ではグリア細胞のアポトーシスが増加し、網膜外核層の厚さと神経細胞の減少を伴い、視細胞死が起こります。基底膜の肥厚と周皮細胞の消失は、DRの基本的な病理変化であり、周皮細胞と内皮細胞の構造的、機能的完全性は網膜毛細血管の安定性を維持する上で重要な役割を担っています。STZ誘発糖尿病動物モデルは、上記の病態変化を再現することができ、DRの初期病態変化の理想的な動物モデルだと言えます。
ウサギでは網膜出血、血管障害、静脈血栓症、増殖性網膜症、サルでは綿状白斑と過蛍光斑を伴う虚血性網膜症、ブタでは網膜BRB透過率の上昇、内顆粒層(INL)と神経節細胞層(GCL)の菲薄化、毛細管基底膜の肥厚を引き起こすことが研究で明らかにされています。STZ誘発DR動物モデルは、病理学的変化という点で一般的な臨床症状をよりよく再現でき、DRの病因と治療に関する研究に予測を提供し、DR研究に広く用いられています[3]。
- 食餌誘発性モデル
食餌誘発性視覚疾患のげっ歯類モデルは、50年前から存在しています。高脂肪・高糖質食を与えたマウスは、6週間で高血糖を起こし、15ヶ月後には網膜内皮細胞が減少し、21ヶ月後には微細動脈瘤と網膜肥厚の病変を発症します。一方、高脂肪・高糖質食を4週間与えたラットでは、錐体細胞の光に対する感度が低下します。しかし、このモデルは発症までに時間がかかり、進行も遅いという欠点がありますが、他のモデルに比べてマウスの寿命が長いという利点があります。そのため、DRの動物モデルとしては、食餌誘発とSTZ注射を組合せたものがより一般的に用いられています。このシミュレーションモデルは、食事によりインスリン抵抗性を誘導した後、低用量のSTZを注射して膵島機能を低下させ、血糖上昇を引き起こすことで2型糖尿病の病態を再現しています。この方法では、網膜の菲薄化や構造障害、血管内皮増殖因子の発現亢進が起こることが研究で明らかになっています。そのため、食餌誘発性動物モデルは、DRの長期観察実験や薬剤スクリーニング実験によく用いられ、日常的な実験に使われることはほとんどありません[4]。
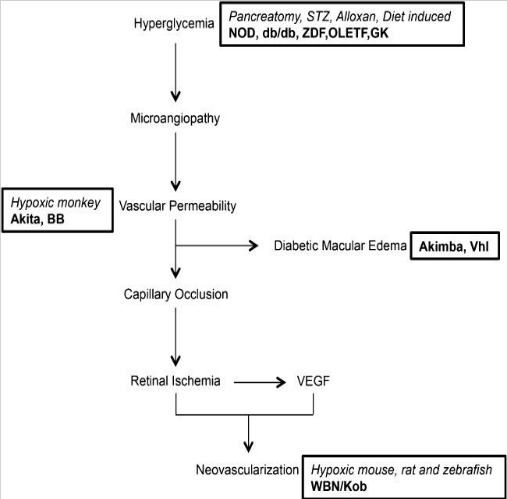
DRの病態と動物モデル[5]
2. DMマウスモデル
糖尿病(DM)は網膜を傷つけ、DRにつながる可能性もあり、両者は密接に関連しています。DMは、明らかに不均一な高血糖とその急性および慢性合併症からなる症候群で、主に遺伝、環境、免疫、その他の要因で引き起こされます。がん、心血管系疾患に次いで、人類の健康を脅かす第三の主要な慢性疾患となっています。米国糖尿病学会(ADA)では、糖尿病を1型糖尿病(T1DM)、2型糖尿病(T2DM)、その他特殊型糖尿病、妊娠糖尿病などに分類しています。糖尿病モデル動物は、糖尿病の研究において重要な役割を担っており、一般に、自然発症性モデル、誘発性モデル、遺伝子改変モデルに分類されます。サイヤジェンは、2型糖尿病マウス(T2DMマウス)、1型糖尿病マウス(T1DMマウス)など、様々な糖尿病モデル、表現型解析サービスを提供しています。
四、サイヤジェン-眼科疾患遺伝子治療薬の開発を加速
眼科遺伝性疾患の患者は、世界的に見ても非常に多くいらっしゃいます。サイヤジェンは、包括的な医薬品開発業務受託機関(CRO)ソリューションプロバイダーとして、上記の障害を克服するためのワンストップ眼科疾患遺伝子治療開発プラットフォームを確立しています。
カスタム動物モデルの分野で16年の経験を持つ当社は、糖尿病網膜症(DR)、網膜色素変性症(RP)、網膜変性、レーバー先天性黒内障2型(LCA2)、レーバー先天性黒内障10型(LCA10)、加齢黄斑変性(ARMD)、角膜内皮ジストロフィーなど眼科疾患を標的とした一連の遺伝子編集モデルについて独自の開発を行っています。
当社は、お客様の前臨床試験(薬効薬理試験)を加速させるために、遺伝子改変動物モデル、完全ヒト化マウスモデル、手術モデルを提供することができます。希少疾患データセンター(RDDC)の支援、確立された技術ルート、多くの成功事例は、サイヤジェンの前臨床眼科研究ソリューションが専門的かつ標準的であることを証明しています。
さらに詳しいサポートが必要な場合は、お気軽にお問い合わせいただくか、[email protected] までプロジェクトの詳細をご連絡ください。
私たちのエキスパートが、あなたの新しい研究モデルをサポートさせていただきます!
参考文献:
[1] Araújo RS, Silva MS, Santos DF, et al. Dysregulation of trophic factors contributes to diabetic retinopathy in the Ins2 mouse [J]. Exp Eye Res, 2020, 194: 108027.
[2] Li CR, Sun SG. Rodent model of spontaneous diabetic retinopathy[J].Int Rev Ophthalmol, 2010, 34(2):119-122
[3] Lai AK, Lo AC. Animal models of diabetic retinopathy: summary and comparison [J].J Diabetes Res, 2013, 2013: 106594
[4] Clarkson-Townsend DA, Douglass AJ, Singh A, et al. Impacts of high fat diet on ocular outcomes in rodent models of visual disease[J]. Exp Eye Res, 2021, 204: 108440
[5] Olivares, A. M., Althoff, K., Chen, G. F., Wu, S., Morrisson, M. A., DeAngelis, M. M., & Haider, N. (2017). Animal Models of Diabetic Retinopathy. Current diabetes reports, 17(10), 93.
