-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
2021年3月25日、ブリストル・マイヤーズ・スクイブ(Bristol Myers Squibb、BMS)は、抗LAG-3モノクローナル抗体relatlimabと抗PD-1モノクローナル抗体Opdivo(nivolumab)の組合せ療法を発表した。治療を受けていない転移性または切除できない悪性黒色腫患者のII/III期臨床試験RELATIVITY-047(CA224-047)を評価した結果、Opdivo単独投与に比べ、患者の無増悪生存期間(progression-free survival,PFS)を著しく改善でき、試験は主要な目標に達成した。世界初の抗LAG-3抗体の臨床III期データになりました。
この試験はアトランダム・二重盲検を採用した:合計714人の患者を1対1の割合でアトランダムに割り当てられ、それぞれ160 mgのrelatlimabと480 mgのOpdivoを組み合わせた薬、または480 mgのOpdivo単独投与を受けた。四週に一回薬を静脈に注射する。今回の試験の第二の目標である全生存期間(overall survival,OS)と奏効率(objective response rate,ORR)はまだ達成されておらず、試験はまだ進行中。安全性においては、現在、一定量の組合せ療法は耐性が良好で、2つの投与群は安定している。

1.LAG-3の概要
リンパ球活性化遺伝子3(Lymphocyte-activation gene 3,LAG-3)は、CD233とも呼ばれ、Triebelとその同僚によって1990年に発見された。LAG-3はⅠ型膜貫通タンパク質で、免疫グロブリン(Ig)スーパーファミリーに属する。主に活性化したT細胞とNK細胞の表面に発現する。
LAG-3はT細胞の抑制性免疫チェックポイントの一つである。PD-1とCTLA-4と同様に、LAG-3はT細胞の増殖、活性化、および安定状態を負に制御できる。ヒトCD4+細胞にLAG-3を阻害することにより、細胞の増殖を促進し、IL-2、IL-4、IFN-γとTNFαの発現を上昇させることができる。さらに,制御性T細胞(Treg)の抑制役割[1]にLAG−3が関与しているとの研究がある。慢性感染や腫瘍環境における場合、長期的な抗原刺激はLAG-3を継続に高発現して、T細胞の疲労(exhaustion)を招く。そのため、LAG-3シグナル伝達経路を阻害することで、T細胞の疲労の回復を促進することができる。
CTLA−4、CD28とは異なり、研究によると、LAG−3はCD4とリガンドMHC IIを競合することによってT細胞活性を制御するのではなく、細胞内ドメインを媒介として直接T細胞に抑制シグナル[4]を伝達するのである。
2.LAG-3構造
人体の中で、LAG3遺伝子は12番染色体(12p13)に位置し、CD4(12p13.31)に近い。また、LAG-3とCD4はタンパク質レベルにおいてただ約20%の同源性ではあるが、タンパク質構造においては同源性が高い。CD4と同様に、LAG-3の細胞外領域にも4つのIg構造のドメイン(D1-D4)が含まれており、D1とD2の間、D3とD4の間に剛性(rigidity)が表示されており、D1-D2とD3-D4の間に相対的な柔軟性(flexibility)が表示されている。
LAG-3のサイトゾル側末端は三つの部分から構成されている:一つのセリンリン酸化サイト、一つの「KIEELE」のモチーフ(motif)、一つのグルタミン酸-プロリンの2ペプチド反復配列(EP repeat)。この中で、「KIEELE」モチーフは高度に保守的であり、LAG-3下流の抑制シグナル伝達に関与している可能性があり、これはこの構造が欠けているLAG-3タンパク質はT細胞に対する抑制を発揮できないためである。
また、LAG−3には可溶型(sLAG−3)も存在する。sLAG-3は選択的スプライシングによって生成され、または膜結合LAG-3のタンパク質分解切断によって生成される。膜結合LAG-3と同様に、sLAG-3はMHC IIと結合することができるが、一部の抗原提示細胞(APC)の脂筏微細構造領域(lipid raft microdomain)のMHC IIとのみ結合するという研究もある。sLAG−3の具体的な機能についてはまだ明確ではないが、樹状細胞(DC)のMHC IIとの結合がDCの成熟と活性化を促進できることを示す研究がある。
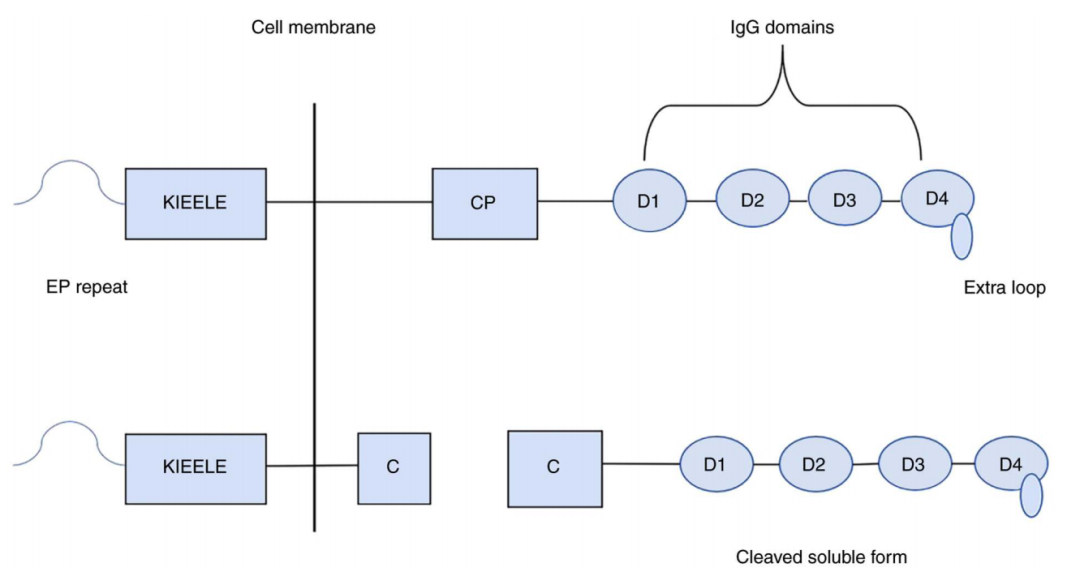
図1.LAG-3とsLAG-3の構造[4]
3.LAG-3のリガンド
CD4と同様に、LAG−3は、主要組織適合複合体II種分子(major histocompatibility complex II、MHC II)と結合することができる。しかし、CD4よりLAG-3とMHC IIの親和力はより高く(約100倍)、それはLAG-3はそのD 1ドメインのうちの30個のアミノ酸からなる環状構造を通じて、MHC IIとの相互作用を強めることができるからである[4、5]。研究によると、LAG−3は安定なペプチド−MHC II分子複合体(pMHC II)と選択的に結合することができ、そのため、LAG−3は安定なpMHCIIのCD4+T細胞の活性化を優先的に抑制することができる[8]。また、MHC IIは主にAPCに発現するが、悪性黒色腫を含む多くの腫瘍細胞もMHC IIを高発現する。それに、この異常的発現は不良予後に関連している。
また、FGL1(fibrinogen-like protein1)もLAG-3の主なリガンドの一つであることを示す研究がある[6]。FGL1は線維素原タンパク質ファミリーに属して、肝細胞から分泌され、多種の腫瘍細胞で高発現する。例えば前立腺癌と悪性黒色腫。
LAG-3はまた、LAG-3のグリカンと相互作用することが可能の2つのリガンドLSECtiとGalectin-3がある。LSECtinはC型レクチンに属し、主に肝臓で発現する。また、多種の腫瘍細胞(悪性黒色腫、膀胱がん、膵がんを含む)はLSECtiを高発現する。Galectin-3はガラクトシドのアドヘシンで、多種の細胞と悪性腫瘍細胞(腫瘍微小環境の中の間質細胞とCD8+T細胞を含む)で発現する。
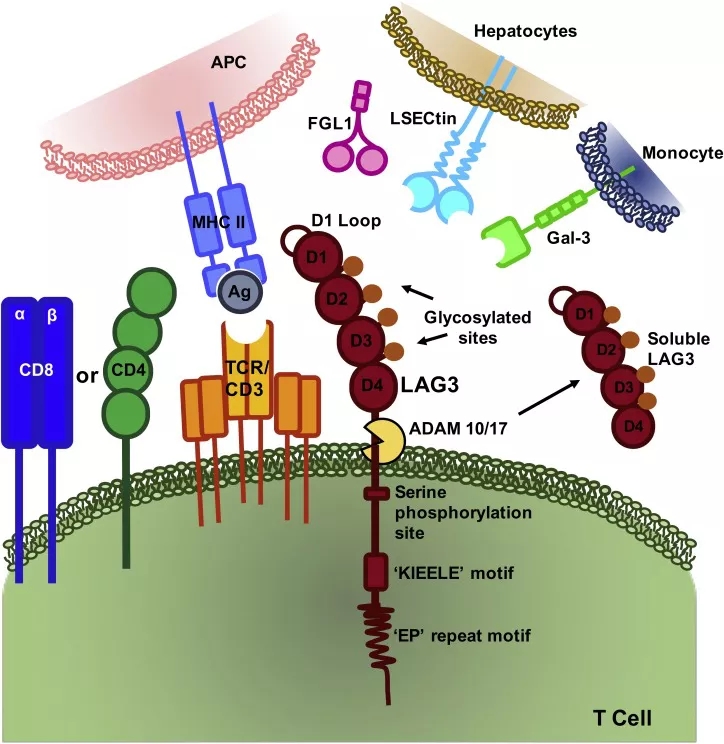
図2.LAG-3の構造とリガンド[7]
4.まとめ
LAG-3は非常に有望な免疫治療標的です。Jonathan Cheng、BMSの副CEOも「免疫チェックポイント抑制剤の単独投与あるいは組み合わせ薬はもう(腫瘍)治療法を変えましたが、依然として、多くの患者が相補的な方法を利用して抗腫瘍活性を増強する新型組み合わせ療法から恵まれる」と話した。現在、PD-1、PD-L1、CTLA-4をターゲティングする抗体薬物が多く開発されましたが、サイヤジェンはより多くの免疫チェックポイントを探して、そのメカニズムを研究して、より効果的な新型免疫療法の開発を目指しています。また、免疫チェックポイント薬物の薬理効果のメカニズムの研究も重要であり、これは薬物応答性の向上、薬物耐性の低下、患者の予後改善に役立ちます。
サイヤジェンの「ノックアウトマウスライブラリ」はLAG-3ノックアウトマウスとLAG-3コンディショナルノックアウトマウスを提供できます。ご興味をお持ちいただけましたら、いつでもお気軽にご連絡ください。
サイヤジェンCTLA-4/LAG3ダブル免疫チェックポイントヒト化マウス
品系バックグラウンド:C57BL/6N
品系構築策略:
hLAG3とhCTLA-4マウスを交配させて、CTLA-4/LAG3ダブル免疫チェックポイントヒト化マウスモデル(hCTLA-4/hLAG3)を得る。hCTLA-4とhLAG3の発現は内因性のマウスのプロモータによって制御される。
品系説明:
- hCTLA-4とhLAG3はマウスの体内で正常な生理発現と調整モードを持っている。
- LAG3とCTLA-4の細胞外領域をヒト化にするのは、hCTLA-4とhLAG3標的医薬の識別に有利である。
- マウスのCTLA-4とLAG3細胞内領域を保留し、正常な細胞内のシグナル伝達を保証する。
- マウス標的遺伝子を発現しないので、交差反応を避けられる。
- マウスの免疫系の機能は健全である。
研究の応用:
このモデルはhCTLA−4及び/或いはhLAG3標的医薬の免疫健全なマウスの体内での有効性と安全性を評価するのに用いられる。
モデル検証:
- CTLA−4の発現検査
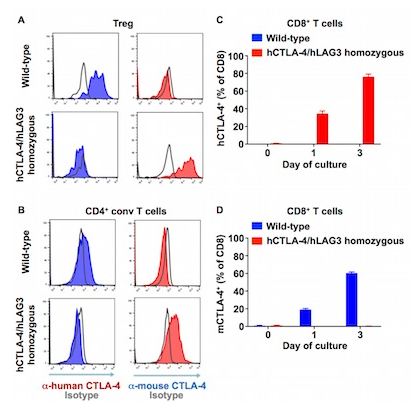
Figure 1. hCTLA 4 expression pattern in hCTLA-4/hLAG3 mice recapitulates mCTLA-4 in wild-type mice. Splenocytes from hCTLA-4/hLAG3 double-homozygous mice were activated with coated αCD3/αCD28 and mIL-2 for 2 days (A, B) or indicated time (C, D). hCTLA-4 and mCTLA-4 expressions were evaluated on A) Tregs (viable, CD3+CD4+CD25+Foxp3+), B) conventional CD4+ (viable, CD3+CD4+Foxp3-), and C, D) CD8+ (viable, CD3+CD8+) T cells.
- LAG3の発現検査
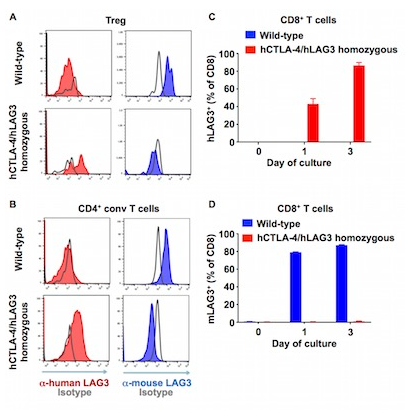
Figure 2. hLAG3 expression pattern in hCTLA 4/hLAG3 double-humanized model. Splenocytes from wild-type or hCTLA-4/hLAG3 double-homozygous mice were activated with coated αCD3/αCD28 and mIL-2 for 2 days (A, B) or indicated time (C, D). hLAG3 and mLAG3 expression on A) Tregs (viable, CD3+CD4+CD25+Foxp3+), B) conventional CD4+ (viable, CD3+CD4+Foxp3-), and C, D) CD8+ (viable, CD3+CD8+) T cells.
hCTLA-4/hLAG 3マウス以外にも、サイヤジェン株式会社はシングル免疫チェックポイントとダブル免疫チェックポイントのヒト化マウスを提供できます。ご興味をお持ちいただけましたら、いつでもお気軽にご連絡ください。
腫瘍は人の健康を脅かす大きな疾患のひとつです。マウス腫瘍モデルは、腫瘍の発生と進行のメカニズム、薬剤のスクリーニングと有効性の評価を研究するための不可欠なツールです。サイヤジェンモード動物イノベーション薬品研究開発プラットフォームは、貴方のニーズに応じて、さまざまな効果的な腫瘍モデルを提供できます。例えば、従来の免疫不全マウスBALB/c nude(ヌードマウス)やNOD scid、免疫チェックポイントヒト化マウス、腫瘍細胞株移植モデル、ヒト由来腫瘍組織異種移植モデル(CDX)、遺伝子修飾モデルおよび表現型分析サービスなど。
私たちはお客様のニーズに合わせるように、さまざまな皮下、イン・サイチュ、または転移性腫瘍モデルを構築し、対応するモデルに対して高度にカスタマイズされたインビボ薬力学的サービスを提供できます。
>> ここをクリックして、動物モデルの検証データをアクセスし、または動物モデルを注文する
参考文献:
[1] Huang C.T., Workman C.J., Flies D., et al. (2004) Role of LAG-3 in regulatory T cells. Immunity. 21(4):503-13.
[2] Shan C, Li X, Zhang J. (2020). Progress of immune checkpoint LAG-3 in immunotherapy. Oncol Lett. 20(5):207.
[3] Brignone, C., Grygar, C., Marcu, M., et al. (2007). A soluble form of lymphocyte activation gene-3 (IMP321) induces activation of a large range of human effector cytotoxic cells. J. Immunol. 179, 4202–4211.
[4] Andrews L.P., Marciscano A.E., and Drake C.G., et al. (2017). LAG3 (CD223) as a cancer immunotherapy target. Immunological reviews 276,1: 80-96.
[5] Huard B., Mastrangeli R., Prigent P., et al. (1997). Characterization of the major histocompatibility complex class II binding site on LAG-3 protein. Proc Natl Acad Sci U S A. 27;94(11):5744-9.
[6] Wang J., Sanmamed M.F., Datar I., et al. (2019). Fibrinogen-like Protein 1 Is a Major Immune Inhibitory Ligand of LAG-3. Cell. 176(1-2):334-347.e12.
[7] Ruffo E., Wu R.C., Bruno T.C.,et al. (2019). Lymphocyte-activation gene 3 (LAG3): The next immune checkpoint receptor. Semin Immunol. 42:101305.
[8] Maruhashi, T., Okazaki, Im., Sugiura, D. et al. (2018) LAG-3 inhibits the activation of CD4+ T cells that recognize stable pMHCII through its conformation-dependent recognition of pMHCII. Nat Immunol . 19, 1415-1426.]
サイヤジェン株式会社について
サイヤジェン株式会社は15年間の発展を経て、すでに全世界の数万人の科学研究者にサービスを提供しており、製品と技術はすでに直接にCNS (Cell、Nature、Science)の定期刊を含む4,800余りの学術論文に応用されています。弊社の「ノックアウトマウスライブラリ」は低価格だけでなく、「遺伝子ID」を検索すれば、ワンクリックで注文まで操作できます。 ノックアウトマウス、ノックインマウス、コンディショナルノックアウトマウス、CRISPR Cas9 ノックアウトマウスのカスタマイズサービスを提供する以外、サイヤジェン株式会社は専門的な手術疾患モデルチームがあり、多種の複雑な小動物手術疾患モデルを提供できます。国際レベルで無菌マウス技術プラットフォームは無菌マウス、無菌動物カスタマイズサービス、微生物移植サービスなどの無菌動物モデルに基づいた各種製品とサービスを提供でき、サイヤジェン株式会社の成熟で安定なトランスジェニックマウスプラットフォームと結合し、遺伝子とフローラの相互機序を研究することもできます。
