-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
1991年、マイケル・J・フォックスの人生が大きく変わりました。大成功を収めた映画「バック・トゥ・ザ・フューチャー」3部作の公開からわずか数ヵ月後、筋肉痛に襲われた俳優は神経科医を訪れ、パーキンソン病と診断されたのです。当時、フォックスは30歳で、キャリア絶頂期にありました。それ以来、彼は時に苦労しながらも、普通の生活を送り、2020年に正式に引退するまで、アルバイトで食いつないできました。[1]
パーキンソン病(PD)とは?重篤な病気とされているのでしょうか?どのようにして発症するのでしょうか?治すことはできるのでしょうか?PDは実はそれほど珍しい病気ではないのですが、しかし、それを語るとなると、まだまだ無数の疑問が残っています。ここでは、世界中で1,000万人が罹患しているこの長期的な神経変性疾患について理解を深めるために、PDとその関連マウスモデルを紹介します。

図1. 2022年10月8日、ニューヨークのコミコンで行われた「バック・トゥ・ザ・フューチャー」のパネルに登場したマイケル・J・フォックス(出典:MIKE COPPOLA (GETTY IMAGES))
パーキンソン病とは?
パーキンソン病(PD)は、主に運動系に影響を及ぼす中枢神経系(CNS)の長期にわたる変性疾患で、イギリスの医師James Parkinsonによって初めて体系的に報告されました。その臨床症状は主に振戦、固縮、動作緩慢、歩行障害であり、非運動症状として睡眠障害、認知障害、うつ病などが挙げられます。[2]
世界で2番目に多い神経変性疾患として、PDの発症率は年々増加しており、PDによる障害や死亡の増加率は、他の神経疾患よりも高くなっています。そのうち、PDによる障害者は580万人で、2000年と比較して81%増加し、死亡した患者は32万9000人で、2000年と比較して2倍となっています。[3]
PDの病因は不明であり、遺伝的要因と環境要因の両方が関与していると考えられています。典型的な症例の診断は主に症状に基づいて行われ、運動症状が主訴となります。PDには治療法が確立されておらず、治療は症状の影響を軽減することを目的としています。
PDの発症メカニズム
PDの臨床病理学的特徴は、中脳の特定部位である黒質緻密部(SNpc)のニューロンの減少、ミスフォールドしたαシヌクレイン(αSyn)の蓄積によるレビー小体(LB)の形成、線条体ドーパミン(DA)欠乏であることが判明されています。[5]現在、PDの発症メカニズムについては、α-シヌクレインのミスフォールディングと凝集、ミトコンドリア機能障害、タンパク質クリアランスの障害、神経炎症、酸化ストレスなどの説が主流となっています。[4]
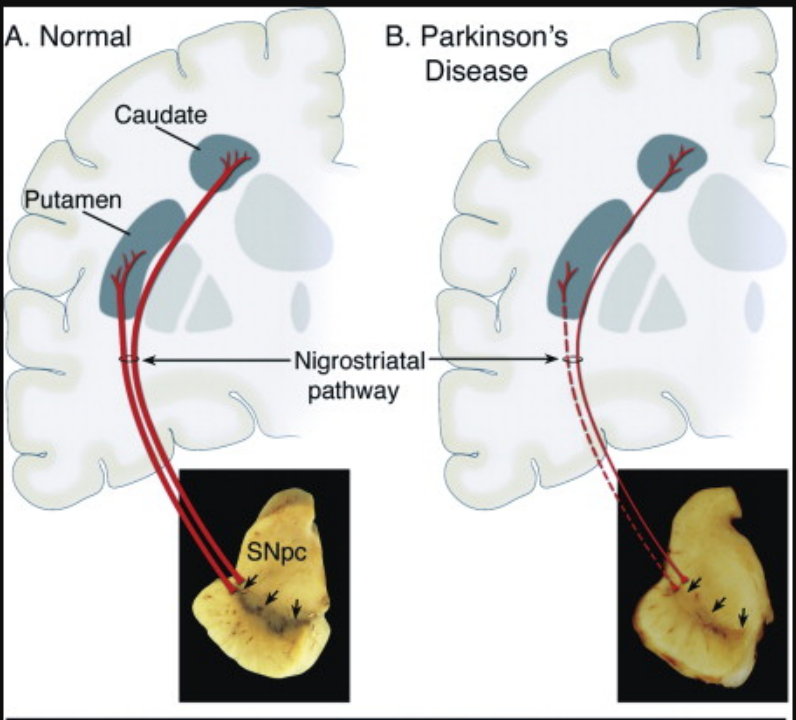
図2 パーキンソン病の神経病理学的特徴
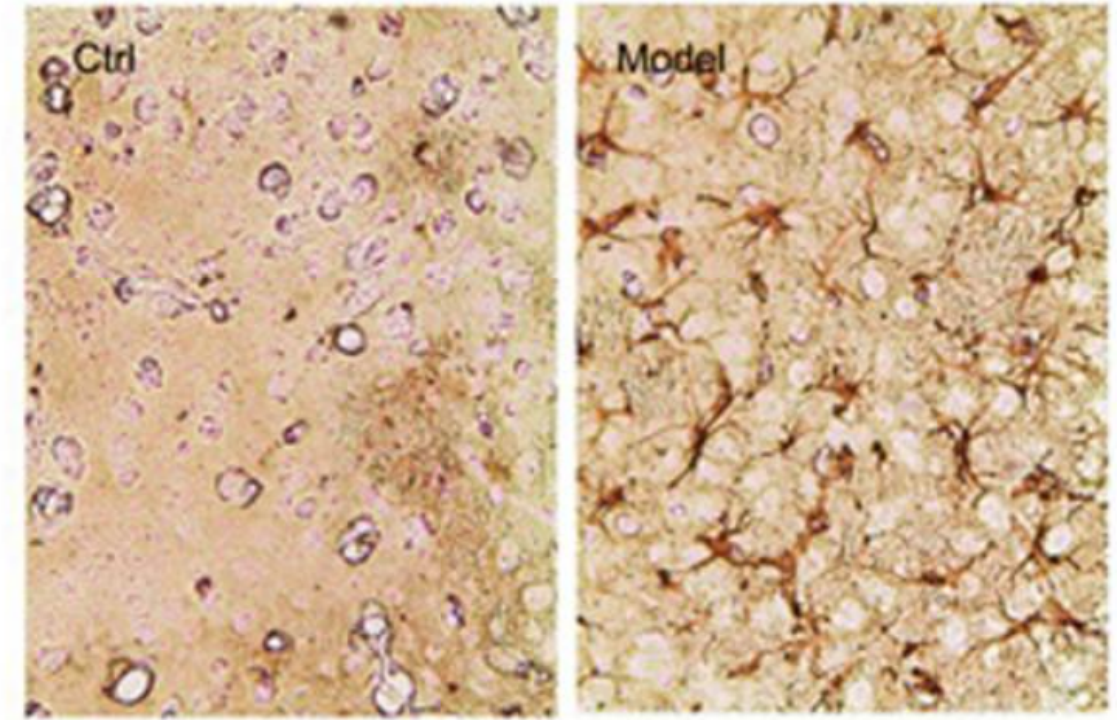
図3 α-Synの蓄積[6]
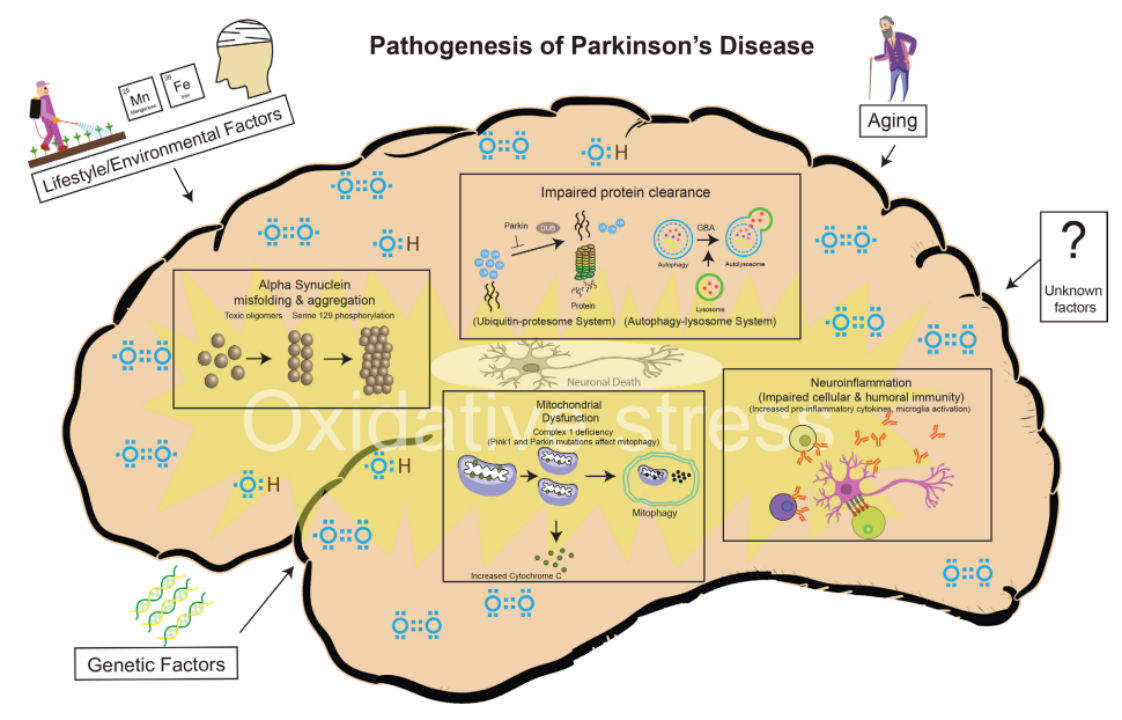
図4 PDの危険因子と発症メカニズム
PDの動物モデル
近年、PDの神経生物学的メカニズム、遺伝的要因、環境的要因について、研究者の間で理解が深まってきています。しかし、医薬品開発への道のりはまだまだ険しい。利用可能なバイオマーカーの不足、優れた創薬ターゲットの不足、原因因子の探索のいずれも創薬開発の進展を妨げています。これらのニーズに応えるために、研究に適した動物モデルの利用は非常に重要です。
PDの動物モデルの作製には、大きく分けて神経毒モデルと遺伝子モデルの2つのアプローチがあり、神経毒モデルと遺伝子モデルを併用した研究も少数ながら存在しますが、その中でも神経毒モデルが最も広く用いられています。[7]
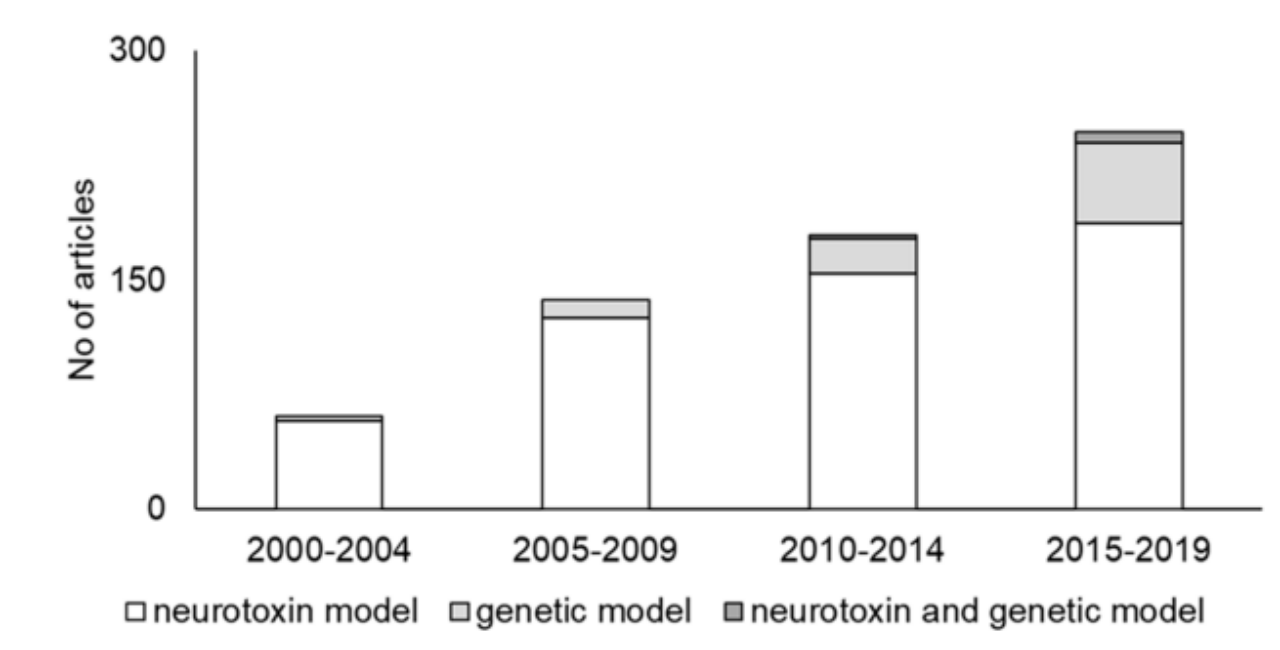
図5 PDの動物モデルの動向文献も徐々に増えてきています。[7]
神経毒モデル[8]
神経毒モデルでは、6-ヒドロキシドーパミン(6-OHDA)や1-メチル-4-フェニル-1,2,3,6-テトラヒドロピリジン(MPTP)が最も広く用いられています。神経毒モデルの作成方法としては、神経毒の全身か、脳内投与が主流とされています。異なる神経毒モデルにより、PDの異なる病理学的特徴をシミュレートすることができます。
6-OHDAの脳内投与によるPDモデル
モデル化:一般に線条体、内側前脳束(MFB)、黒質(SN)の部位で注射が行われます。通常、それらの注射部位のDAニューロンのアポトーシスは3-5日後に検出できます。線条体に6-OHDAを注射すると、線条体の軸索終末が破壊され、次いでSNでドーパミン作動性ニューロンの変性・脱落します。症状は比較的軽く、進行も緩やかです。しかし、従来の標的であるMFBやSNに6-OHDAを注射すると、急速かつ大量のドーパミン作動性細胞の変性が引き起こされてしまいます。
表現型の特徴:このPDモデルは、行動障害に関しては臨床的表現型と一致し、PDの非運動症状を発症しますが、LB形成という病理学的表現型は欠落しています。
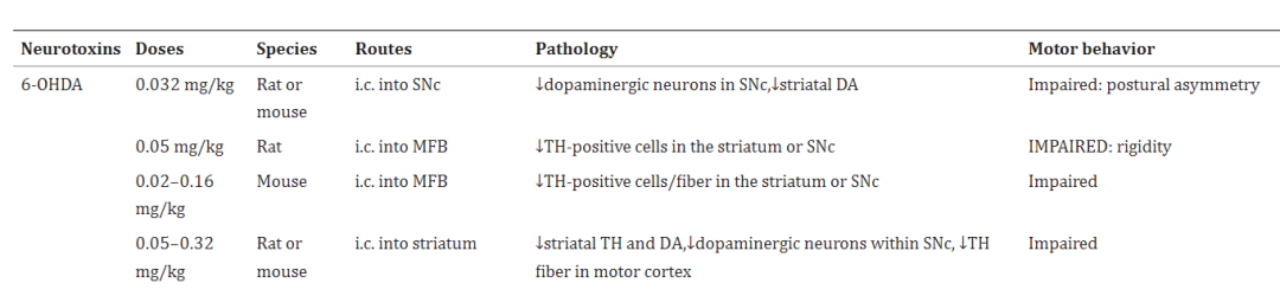
図6 6-OHDAの投与経路とげっ歯類のパーキンソン病[8]
MPTPの脳内または末梢注入により誘導されたPDモデル
モデル化:MPTP は親油性分子であり、血液脳関門を容易に通過することができます。全身あるいは脳内投与後、MPTPはアストロサイトのモノアミン酸化酵素B(MAOB)により酸化され、強力なドーパミン神経毒である1-メチル-4-フェニルピリジニウムイオン(MPP+)に変化することができます。MPP+ は、ドーパミンと構造が似ているため、ドーパミントランスポーター(DAT)を介してドーパミン作動性ニューロンに容易に取り込まれる毒性代謝物です。[9]その後、MPP+ は、線条体ドーパミンレベルの低下とともに、SNにおけるDA ニューロンのアポトーシスを誘導します。[10]DAニューロンのアポトーシスのメカニズムは、MPP+がミトコンドリア呼吸における呼吸鎖複合体Iを阻害することにより、線条体およびSNにおけるATP濃度が急激に低下し、DAニューロンがアポトーシスを起こすと考えられています。[11]
表現型の特徴:MPTPを全身投与すると、線条体や黒質のDAニューロンの消失、脳の酸化ストレス、ミトコンドリア機能障害など、PDの進行性の病態が顕在化しますが、しかし、このモデルもLB形成という病的表現型を欠如しています。[8]既存の神経毒モデルでは、ロテノン誘発PDモデルでLB形成の病的表現型を観察することができます。[12]
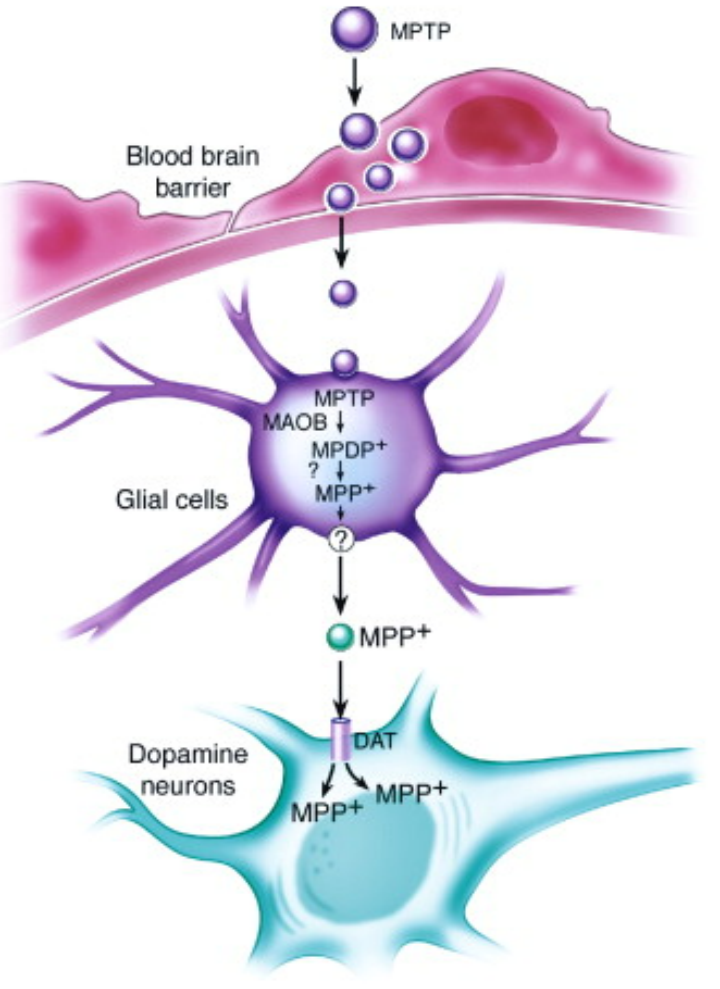
図7 MPTPによるDAニューロンのアポトーシスのメカニズム[5]
遺伝子モデル[13]
また、PDの発症には遺伝も重要な役割を担っています。家族性PDと特発性PDの解析により、SNCA、Parkin、DJ-1、PINK1、LRRK2が病因遺伝子として同定されました。
|
遺伝子名 |
遺伝子機能 |
対立遺伝子 (アレル) |
利点 |
制限 |
|
SNCA |
α-シヌクレインのコード化 |
変異型(A53T, A30P, E46K)または重複する断片 |
α-シヌクレインが関与する変性疾患や、PDの遺伝要因と環境要因の関連性などの研究に利用できます。 |
モデルによっては、ドーパミン作動性ニューロンの著しい減少が見られないものや、ヒトのPD病理学と矛盾するアポトーシスのパターンを示すものもあります。 |
|
LRRK2 |
家族性PDの原因遺伝子 |
変異型(G2019SとR1441C/G) |
LRRK2標的治療の試験やLRRK2機能研究などに利用できます。 |
このモデルは運動障害を示したが、顕著なドーパミン作動性ニューロンの変性喪失、LB形成の欠如は認められませんでした。 |
|
Parkin |
ユビキチンリガーゼのコード化;変異やノックアウトにより神経毒性基質が蓄積される可能性があります。 |
変異、ノックアウト |
Parkin機能研究に利用できます。 |
このモデルには、表現型データが欠如しています。 |
|
DJ-1 |
抗酸化タンパク質のコード化 |
ノックアウト |
神経毒モデルと併用可能。 |
このモデルは運動障害を示すものの、LB形成を欠如しており、ドーパミン作動性ニューロンの著しい損失はなく、表現型データも不足しています。 |
|
PINK-1 |
神経保護キナーゼのコード化 |
変異、ノックアウト |
G309D-PINK1マウスは、ドーパミン減少、運動障害の表現型を示します。 |
ほとんどのPINK-1モデルでは、ドーパミン作動性ニューロンとドーパミンレベルの減少は認められませんでした。 |
PD研究のを加速させるサイヤジェンマウス
PD研究を加速させるために、サイヤジェンはPD関連遺伝子のKO/CKOマウス系統をご提供しています。以下の表のリンクより、対応する製品情報および系統の説明をご覧いただけます。
|
遺伝子名 |
技術タイプ |
系統 |
製品詳細 |
|
Snca |
KO |
C57BL/6N-Sncaem1Cya |
|
|
Snca |
cKO |
C57BL/6J-Sncaem1(flox)Cya |
|
|
Lrrk2 |
KO |
C57BL/6J-Lrrk2em1Cya |
|
|
Lrrk2 |
cKO |
C57BL/6J-Lrrk2em1(flox)Cya |
|
|
Park7 |
KO |
C57BL/6J-Park7em1Cya |
|
|
Park7 |
cKO |
C57BL/6J-Park7em1(flox)Cya |
|
|
Pink1 |
KO |
C57BL/6J-Pink1em1Cya |
|
|
Pink1 |
cKO |
C57BL/6N-Pink1em1(flox)Cya |
動物モデル支援パッケージをお探しですか?サイヤジェンの神経行動学プラットフォームには、ネズミの行動評価、行動試験装置、専門的な記録・解析システムに利用できるスペースがあり、水迷路、NORT、Y迷路、ロータロッド、OFT、FST、EPM、その他の種類のラットやマウスの行動試験サービスをご提供できます。
ご連絡いただければ、モデルデザインスペシャリストがプロジェクトのニーズを迅速にお伺いします。または、[email protected] まで、サービスに関するお問い合わせやお見積り依頼について、お気軽にご連絡ください。
References:
[1] “Michael J. Fox: ‘I’m 61 years old, and I’m feeling it a little bit more’”. Andrea Jimenez. Elpais. 28 Oct 2022.
[2] Poewe W, Seppi K, Tanner CM, Halliday GM, Brundin P, Volkmann J, Schrag AE, Lang AE. Parkinson disease. Nat Rev Dis Primers. 2017 Mar 23;3:17013. doi: 10.1038/nrdp.2017.13. PMID: 28332488.
[3] World Health Organization, https://www.who.int/newroom/fact-sheets/detail/parkinson-disease.
[4] Jankovic J, Tan EK. Parkinson's disease: etiopathogenesis and treatment. J Neurol Neurosurg Psychiatry. 2020 Aug;91(8):795-808. doi: 10.1136/jnnp-2019-322338. Epub 2020 Jun 23. PMID: 32576618.
[5] Dauer W, Przedborski S. Parkinson's disease: mechanisms and models. Neuron. 2003 Sep 11;39(6):889-909. doi: 10.1016/s0896-6273(03)00568-3. PMID: 12971891.
[6] Zhang QS, Heng Y, Mou Z, Huang JY, Yuan YH, Chen NH. Reassessment of subacute MPTP-treated mice as animal model of Parkinson's disease. Acta Pharmacol Sin. 2017 Oct;38(10):1317-1328. doi: 10.1038/aps.2017.49. Epub 2017 Jun 26. PMID: 28649132; PMCID: PMC5630672.
[7] Kin K, Yasuhara T, Kameda M, Date I. Animal Models for Parkinson's Disease Research: Trends in the 2000s. Int J Mol Sci. 2019;20(21):5402. Published 2019 Oct 30. doi:10.3390/ijms20215402
[8] Zeng XS, Geng WS, Jia JJ. Neurotoxin-Induced Animal Models of Parkinson Disease: Pathogenic Mechanism and Assessment. ASN Neuro. 2018 Jan-Dec;10:1759091418777438. doi: 10.1177/1759091418777438. PMID: 29809058; PMCID: PMC5977437.
[9] Marti Y., Matthaeus F., Lau T., Schloss P. Methyl-4-phenylpyridinium (MPP+) differentially affects monoamine release and re-uptake in murine embryonic stem cell-derived dopaminergic and serotonergic neurons. Mol. Cell. Neurosci. 2017;83:37–45. doi: 10.1016/j.mcn.2017.06.009.
[10] Bezard E., Gross C.E., Fournier M.C., Dovero S., Bloch B., Jaber M. Absence of MPTP-induced neuronal death in mice lacking the dopamine transporter. Exp. Neurol. 1999;155:268–273. doi: 10.1006/exnr.1998.6995.
[11] Sayre L.M., Wang F., Hoppel C.L. Tetraphenylborate potentiates the respiratory inhibition by the dopaminergic neurotoxin MPP+ in both electron transport particles and intact mitochondria. Biochem. Biophys. Res. Commun. 1989;161:809–818. doi: 10.1016/0006-291X(89)92672-7.
[12] Inden M., Kitamura Y., Abe M., Tamaki A., Takata K., Taniguchi T. Parkinsonian rotenone mouse model: Reevaluation of long-term administration of rotenone in C57BL/6 mice. Biol. Pharm. Bull. 2011;34:92–96. doi: 10.1248/bpb.34.92.
[13] Chia SJ, Tan EK, Chao YX. Historical Perspective: Models of Parkinson's Disease. Int J Mol Sci. 2020 Apr 2;21(7):2464. doi: 10.3390/ijms21072464. PMID: 32252301; PMCID: PMC7177377.
