-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
非アルコール性脂肪性肝炎(nonalcoholic steatohepatitis, NASH)は、栄養過剰による肝臓の脂肪変性と慢性炎症によって引き起こされる肝臓の代謝性疾患であり、徐々に肝線維化、肝硬変、さらには肝細胞癌に発展します。現在、NASHの治療のために承認された薬はありません。最近の研究では、AMPK経路を活性化することにより、コルジセピンが肝臓の脂肪蓄積を抑制し、肝臓の炎症性損傷や線維化の発生を予防できることがわかりました。この研究成果は2021年2月にHepatology (IF=14.679,Q1) 雑誌に発表されました。

コルジセピン(Cordycepin)は冬虫夏草の主要な活性成分であり、抗炎症、抗酸化、抗線維化、抗脂肪生成、抗腫瘍など、幅広い生物学的活性を持っています。ただし、NASHの進行に対するコルジセピンの役割およびその根本的なメカニズムはまだ不明です。そのため、研究チームは、高脂肪食(HFD)と高脂肪高コレステロール食(HFHC)を与えることにより、NASHマウスモデルを確立し(この2つのモデルはヒトNASHの代謝特徴をカバーしている)、NASHの発生と発達に対するコルジセピンの影響を調査しました。
1. コルジセピンは、パルミチン酸によって誘発される肝細胞の脂質蓄積、炎症、脂肪毒性を軽減することができます
代謝ストレス下での肝細胞脂質蓄積および炎症に対するコルジセピンの影響を研究するために、混合脂肪酸PO(パルミチン酸、PAおよびオレイン酸、OA)によってLO2細胞を刺激しました。結果は、コーディセピンが細胞内脂肪滴蓄積、トリアシルグリセロール(TG)および血清総コレステロール(TC)含有量、脂肪酸合成(FASN、SCD1、ACCα、PPARγ)および炎症(IL-6、TNFα、CCL5、CXCL10)関連遺伝子の発現を効果的に減少させたことを示しています。肝細胞に対するコルジセピンの影響を体系的に評価するために、肝細胞のRNA-Seq分析を行った結果、グループ間の差次的遺伝子が炎症、脂質代謝およびアポトーシス関連経路に有意に富み、かつ、コルジセピンが、上記の経路に有意に富んだ差次的遺伝子の発現を有意にダウンレギュレートすることができることを示しています。
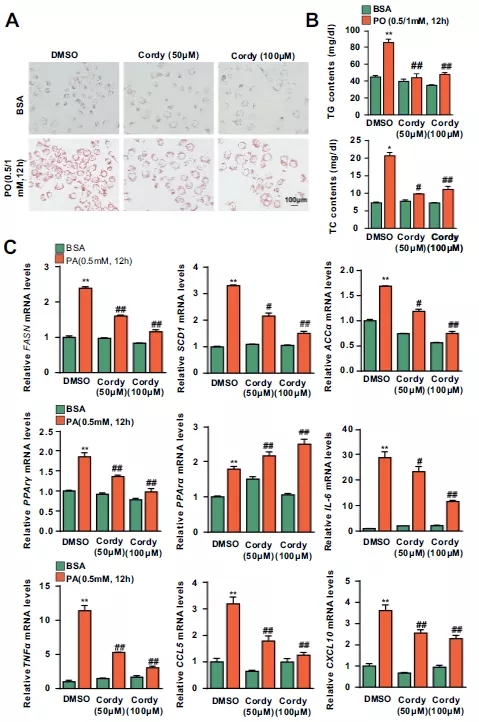
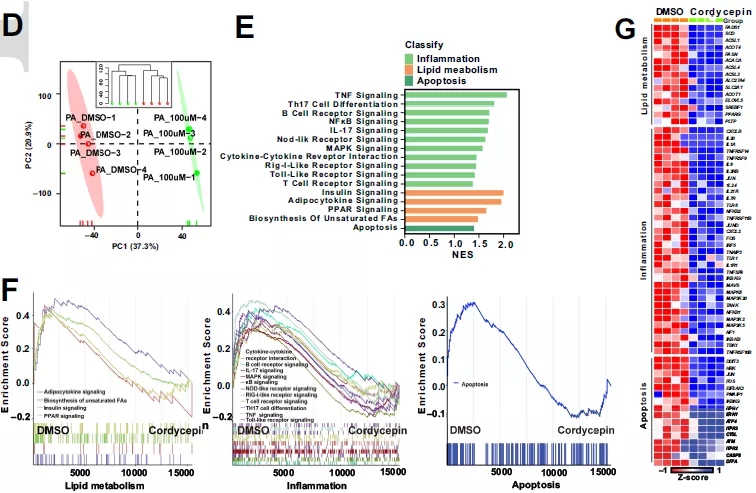
図1. 肝細胞の脂質蓄積と炎症に対するコルジセピンの影響。
2. コルジセピンは、高脂肪食によって引き起こされる肝臓の脂肪変性と炎症を軽減することができます
コルジセピンがHFDによって引き起こされたマウスのNASH疾患(雄C57BL/6JマウスHFDに24週間摂食させる)を軽減できるかどうかを調査しました。実験結果は、コーディセピンがHFDによって引き起こされた肝臓指数の増加、肝臓脂質(TG、TC)含有量の増加、肝臓の病理学的損傷(脂質蓄積、 気球状変性、炎症性浸潤)、脂肪酸合成摂取、および炎症反応関連遺伝子と蛋白質の発現を有意に減少させたことを示しています。
3. コルジセピンは、HFHC飲食によって引き起こされた肝臓の脂肪変性、炎症、線維化を改善することができます
インビボでのNASHに対するコルジセピンの保護効果をさらに研究するために、高脂肪および高コレステロール食によって誘発されるマウスNASHモデル(雄C57BL/6JマウスHFHCに16週間摂食させる)を構築しました。このモデルは、HFD誘発モデルよりも重毒な炎症反応と線維化を示しました。結果は、コーディセピンがHFHCによって引き起こされた肝臓指数の増加、肝臓脂質(TG、TC)含有量の増加、肝臓の病理学的損傷(脂質蓄積、 気球状変性、炎症性浸潤と線維化)、脂肪代謝、炎症反応と線維化関連遺伝子と蛋白質の発現を有意に減少させたことを示しています。

図2.NASHマウスのHFHC誘発性脂肪肝、炎症、線維化に対するコルジセピンの影響。
4. 代謝ストレスの間、コルジセピンは肝細胞とマウス肝臓のAMPKシグナルを活性化することができます
NASHに対するコルジセピンの保護メカニズムをさらに調査するために、細胞とマウスのRNA-Seqの結果に対して経路に富むようにした結果、差次的遺伝子が主に脂質代謝、炎症、線維化とアポトーシス経路に集中し、そのうち、 AMPK経路に対するコルジセピンの影響がほかのシグナル経路よりも優れていることが分かりました。マルチオミックス(トランスクリプトミクス、プロテオミクス、およびリン酸化プロテオミクス)分析は、AMPK経路が脂質代謝、炎症、線維化、およびアポトーシスの標的に有意に関連しており、コーディセピン役割の重要な経路である可能性があることを示しています。コルジセピンの抗NASHがAMPK経路を介しているかどうかを判断するために、研究者は、細胞中、HFDとHFHCによってそれぞれ誘発されたマウスの肝臓におけるAMPK経路でのタンパク質発現を測定し、コルジセピンがAMPKおよびその下流のACC蛋白質のリン酸化を有意に活性化することを発見しました。

図3.トランスクリプトームおよびリン酸化プロテオミクス分析:AMPK経路がコルジセピンの標的である可能性があります。
5. AMPKリン酸化を阻害すると、コルジセピン媒介性脂肪毒性肝細胞およびHFD誘発性NASHマウスにおける脂質蓄積および炎症抑制を排除することができます
コルジセピンの抗NASHにおけるAMPKの重要な役割をさらに研究するために、研究者はAMPKノックアウトLO2細胞を構築しました。結果は、AMPK-KO LO2細胞では、AMPK経路の活性化と脂質蓄積に対するコルジセピンの阻害効果が基本的に消失したことを示しました。同時に、AMPK阻害剤Compound CをLO2細胞とHFDで摂食させたマウスに投与した結果、Compound Cによって細胞とマウスに対するコルジセピンの保護効果が完全に排除されたことが示されました。一般に、コルジセピンは、主にAMPKαを介した脂質低下、抗炎症および抗線維化を活性化することにより、その抗NASH効果を発揮します。

図4. LO2細胞でAMPKをノックアウトした後の細胞脂質代謝に対するコルジセピンの影響。

図5. AMPK阻害剤投与後の細胞およびマウスの肝臓の脂肪変性および炎症に対するコルジセピンの影響。
要するに、この研究では、HFDおよびHFHC食によってそれぞれ誘発されたNASHマウスモデルを使用してコルジセピンの抗NASH薬効作用を証明すると同時に、AMPK遺伝子ノックアウト細胞およびAMPK阻害剤で処理した細胞とマウスを使用してコルジセピンの抗NASHの作用機序を明らかにしました。この研究では、研究者らは、コルジセピンがAMPKα阻害剤である可能性があり、AMPK経路を活性化することにより、肝臓の脂肪変性、炎症、線維化を軽減し、それによって非アルコール性脂肪性肝炎の発生を阻害することを発見しました。
非アルコール性脂肪性肝疾患(NAFLD)は、アルコール乱用のない肝疾患症候群であり、単純な脂肪肝、脂肪性肝炎、脂肪性肝線維化、肝硬変などが含まれています。単純な脂肪肝から非アルコール性脂肪性肝炎(NASH)を経て、肝線維化に至るまで発症し、さらには肝硬変、肝細胞癌(HCC)または肝不全などの末期肝疾患につながることもあります。動物モデルは、非アルコール性脂肪肝の病理学および生理学的メカニズムの解明と新薬の開発に重要な役割を果たしています。前臨床研究では、研究される特定のNAFLD表現型に基づいてさまざまな動物モデルを使用する必要があります。NAFLDおよびNASHの前臨床動物モデルは、食事誘発モデル、化学物質誘発モデル、遺伝子編集モデル、および複合モデルの4つのカテゴリに分類できます。
サイヤジェンは、さまざまな非アルコール性脂肪性肝マウスモデルおよび表現型分析サービスを提供できます。必要に応じてあなたの研究のためにカスタマイズできるため、当社までお問い合わせください。
✓ 食事誘発モデル
✓ 遺伝子編集モデル
✓ 複合モデル
オリジナルの検索:
Lan T , Yu Y , Zhang J , et al. Cordycepin ameliorates nonalcoholic steatohepatitis via activation of AMP‐Activated Protein Kinase signaling pathway[J]. Hepatology. 2021.DOI: https://doi.org/10.1002/hep.31749.
関連記事:
>>「サイヤジェン報告書」非アルコール性脂肪性肝疾患動物モデルの概要
サイヤジェン株式会社について
サイヤジェン株式会社は15年間の発展を経て、全世界の数万人の科学研究者にサービスを提供しており、製品と技術は直接にCNS (Cell、Nature、Science)の定期刊を含む5,200余りの学術論文に応用されています。弊社の「ノックアウトマウスライブラリ」は低価格だけでなく、遺伝子名称を入力すれば、ワンクリックで注文まで操作できます。 ノックアウトマウス、ノックインマウス、コンディショナルノックアウトマウス、トランスジェニックマウス、GFPマウス、免疫不全マウス、無菌マウスなどのカスタマイズサービスを提供する以外、専門的な手術疾患モデルチームがあり、多種の複雑な小動物手術疾患モデルも提供できます。
