-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
ウイルスやガンとの長い戦いで、気力を失ったT細胞は徐々に機能を失い、この状態をT細胞枯渇という。現在の人気免疫治療方法の中で、検査点遮断は腫瘍浸润CD8+ Tリンパ細胞の増殖を促進する。しかし、この現象の裏にあるメカニズムは未だに明確ではない。
スイス・ローサン大学のWerner Held氏がリードする研究チームが腫瘍内のTcf1+PD−1+CD8+ T細胞を鑑定された。これらの細胞は幹細胞のような特徴を表し、治療性ワクチンの接種と免疫検査点遮断免疫療法に応え、腫瘍制御を促進する。
この「Intratumoral Tcf1+PD-1+CD8+ T Cells with Stem-like Properties Promote Tumor Control in Response to Vaccination and Checkpoint Blockade Immunotherapy」と題する文章は1月15日付けの「Immunity」誌に掲載された。
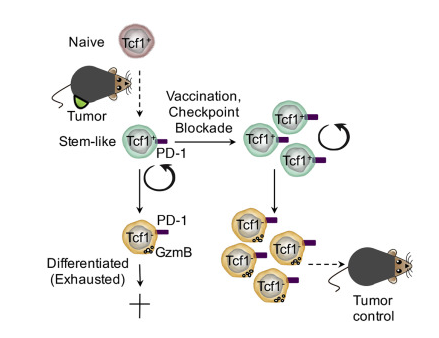
文章概要
検査点遮断は腫瘍浸潤CD8+ Tリンパ細胞(TIL)の増殖反応を介した。このような反応の起源はまだ不明である。慢性活性化がT細胞の最終的な分化、つまりT細胞の枯渇を促進した。研究者は今回腫瘍反応性TILの亜群を鑑定した。それらは枯渇細胞と中枢記憶細胞のマークを示し、つまり検査点タンパク質PD-1と転写因子Tcf1を発現する。
彼らはTcf1+PD-1+ TILが免疫治療時の増殖反応を介して、Tcf1+PD-1+細胞と分化したTcf1−PD-1+細胞が産生することを発見した。Tcf1+PD-1+ TILの消融が免疫治療に対する応答を制限する。Tcf1はTcf1+PD-1+ TILを生成するのに必要ではないが、これらの細胞の幹細胞様機能を維持するのには必要である。
彼らはメラノーマ患者の血液の腫瘍反応性CD8+ T細胞と原発性メラノーマのTILから人類Tcf1+PD−1+細胞を検出した。そのため、免疫検査ポイントの遮断はT細胞の枯渇プログラムの逆転に依存せず、幹細胞様TIL亜群の増殖に依存する。
背景
CD8+ T細胞はある腫瘍での浸潤程度が患者の総生存率を予測でき、リンパ細胞は腫瘍の成長を制限できると表明する。それにもかかわらず、大部分の浸潤腫瘍には進展が見られ、このような自発的な抗腫瘍免疫反応は通常腫瘍を制御するのに不十分であることがわかった。免疫療法は腫瘍の免疫応答を増強して持続的な制御を誘導することを目的としている。現在の方法は養子性T細胞治療と抑制性受容体(免疫検査点)の遮断が含まれる。
ウイルスや腫瘍との長期的な対抗で、T細胞の機能は徐々に失う(いわゆる「T細胞枯渇」)。それらは機能を失い、T細胞の機能の逆向調整剤PD-1を誘導する。一般的にこの種類の枯渇の表現型は終末分化した細胞と考えられる。それらは増殖能力を失い寿命が短い。しかし、PD−1を遮断すると腫瘍のCD8+ T細胞が増殖する。これは終末分化という概念と矛盾している。
このため、研究者は自発または免疫治療による抗腫瘍CD8+ T細胞の反応が記憶性CD8+ T細胞のコンポーネントにつながっているかどうかを知りたい。
Tcf1の欠乏は腫瘍制御を弱化させる
CD8+ T細胞が腫瘍の反応に記憶成分が関与しているかどうかを確定するため、研究者がこれらの反応が転写因子Tcf1に依存しているかどうかを検出した。これは中枢記憶性CD8+ T細胞の形成および機能にとって重要である。彼らは野生型WT或いはTcf7−/−CD8+ T細胞を幼若C57BL/6 (B6)マウスに移動させた。1日後、このP14キメラマウスの皮下にLCMV gp33を発現するB16メラニン腫細胞を注入する。この方法は腫瘍特異性のCD8+ T細胞を追跡するのに用いられ、且つこれらの細胞およびその亜群が腫瘍制御に関わっているかどうかを確認することができる。
腫瘍が接触できる時、彼らはgp33ペプチドを利用してマウスを免疫する。ワクチン接種及びWT或いはTcf7-/ P14细胞の组み合わせで、腫瘍が約1週間後に暫く消える。彼らはWT P14細胞に比べて、Tcf7−/ P14細胞の保護作用は短いことを発見した。治療の終点でWTの中で腫瘍浸潤CD8+ Tリンパ細胞の豊度はTcf7−/−P14より10倍も高かった。そのため、Tcf7を欠乏するP14 TILはワクチン接種の初期に豊度が高かったが、その後に下がり、これが腫瘍制御の減少につながっている。
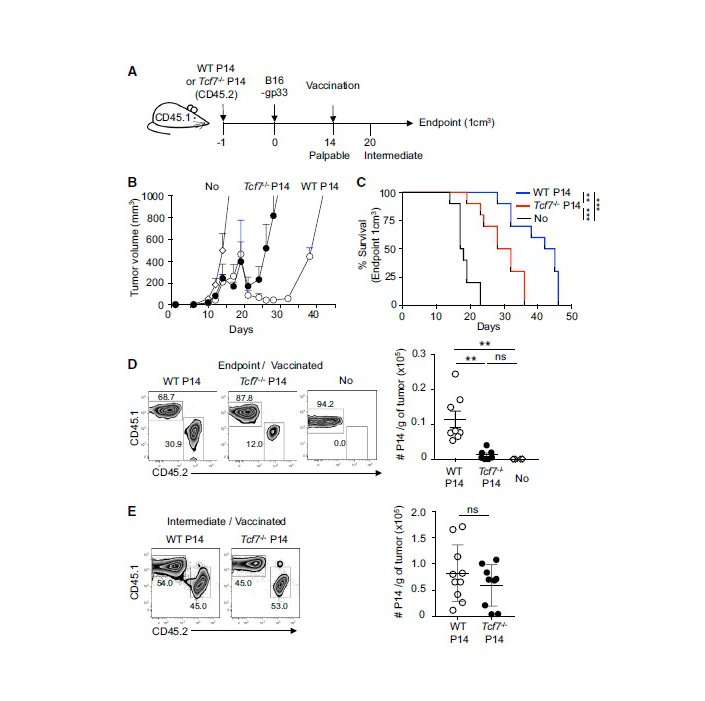
腫瘍特異性TILは大量のTcf1+PD-1+ とTcf1-PD-1+ CD8+ T細胞を含む
延長された腫瘍制御はTcf1に依存するので、その後、研究者はワクチン接種を受けた未治療のマウスのWT P14細胞のTcf1の発現を鑑定した。幼若P14细胞は均一的なTcf1+と表現する。同様に、治療されていないマウスにタッチ可能な腫瘍が現れる時、大部分のP14 TILはTcf1+であるが、PD-1も発現する。腫瘍がミディアムサイズである時、Tcf1+PD-1+ P14 TILは豊度が8倍に増加する。腫瘍が1 cm3に増加する時、その豊度が下がる。
彼らは腫瘍ができたマウスに治療用ワクチンを接種して1週間後にTcf1+PD-1+ P14 TILが急増した(176倍)。また、これらの細胞は終点に依然として非常に高い数で存在している。P14 TILはまた相当の量のTcf1-PD-1+亜群を含む。それらはTcf1+PD-1+ TILと並行して拡大と減少する。GFPマークの実験で、彼らもTcf1+PD-1+ TILが構成的に腫瘍に存在することを発見した。腫瘍の進展に伴い、それらの豊度が急に増加し、且つ治疗用ワクチンの接種によってさらに拡大した。
Tcf1+CD8+ T細胞は腫瘍制御での機能
腫瘍特異性Tcf1+CD8+ T細胞の免疫応答と腫瘍制御における重要性を評価するために、研究者はサイヤジェン株式会社(Cyagen)に依頼して一種類のマウス品系を生成し、体内でTcf1を発現する細胞を選択的に消融させる。彼らはジフテリア毒素受容体(DTR) T2A GFP融合遺伝子をTcf7遺伝子座を含むBACに挿入し、Tcf7DTR−GFP遺伝子組み換えマウスを調製した。続いて、彼らはTcf7DTR−GFP P14キメラマウスを生成し、且つB16−gp33腫瘍細胞を移植した。ジフテリア毒素(DT)処理はGFP+ P14 TILを効果的に除去できるが、GFP−P14 TILの豊度には影響を及ぼさない。
彼らはDTを用いて荷瘤マウスを処理し、且つ再度に免疫接種した。DT露顕はGFP或いはTcf1タンパク質を発現するP14細胞がほぼ消えられ、Tcf1−P14細胞の豊度も低下した。これはTcf1+細胞がTcf1−TILの生成を維持したことを表明した。Tcf7DTR−GFP P14キメラマウスが殺される時に腫瘍の大きさと重さとも低い。これに比べて、Tcf1+ P14細胞が溶けた時には腫瘍が進展することが出現した。これらのデータは腫瘍特異性Tcf1+PD-1+ CD8+ T細胞が抗腫瘍免疫力を形成するのに必要であることを示している。
このように、治療性ワクチンの接種による腫瘍制御はTcf1+PD-1+CD8+ T細胞の存在に依存する。その後、研究者は一連の実験を通じて、外周細胞ではなく、腫瘍内の細胞の貢献を確認した。
免疫検査点遮断療法への呼応
動物モデルとがん患者で、共抑制受容体(例えば、PD-1とCTLA-4)の遮断はT細胞に依存する腫瘍消去を介することができる。しかし、このような治療関与の裏にある分子メカニズムはまだ明らかではない。研究者はTcf1+ CD8+ T細胞が免疫検査ポイント遮断療法で機能する可能性があると予測した。
彼らはTcf7DTR−GFP P14キメラマウスを使用し、FTY720を使って新しいT細胞の腫瘍への流入を防止し、且つジフテリア毒素(DT)を使ってTcf1+ P14 TILを消融した。対照マウスに比べて、検査ポイント遮断療法はTcf1+とTcf1−P14 TILの豊度を10倍以上に増加させた。Tcf1+ TILの消去はTcf1−P14 TILの豊度を大幅に減少した。そのため、検査ポイント遮断は腫瘍のTcf1+ TILを拡張し、これらの細胞は分化のTcf1−TILを生成するのに必要である。
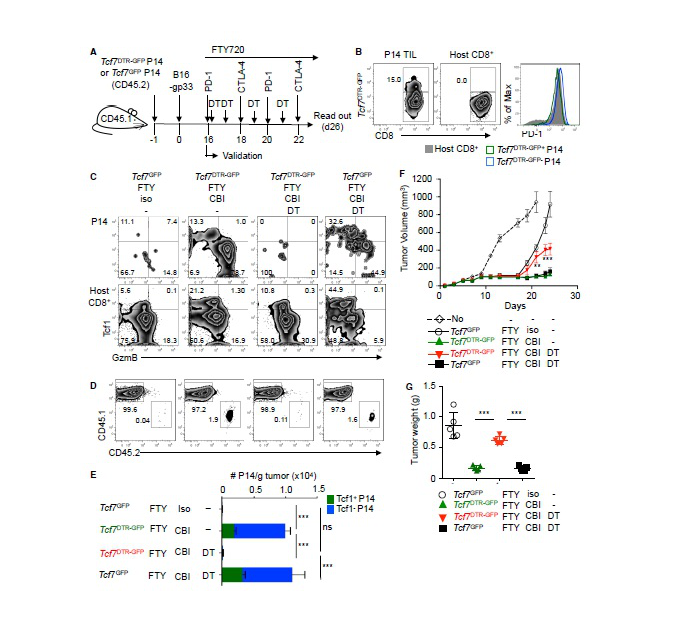
腫瘍のTcf1+PD-1+CD8+ T細胞は幹細胞と枯渇細胞の特徴を持っている
Tcf1+PD-1+ TILの腫瘍制御への重要性を考えると、研究者はこれらの細胞の分子鑑定を行った。彼らは機能分析により、Tcf7GFP+ TILはTcf7GFP+細胞を拡張、分化、再生する潜在力があることを発見した。幹細胞様特徴と同じ、RNA-seq分析もTcf7GFP+ P14 TILの転写本が成体幹細胞或いは造血幹細胞の発現する遺伝子の一部と明らかに重なることも発見した。同時に、Tcf7GFP+ TILも複数の枯渇マーク物質(Pdcd1)を発現したが、Tcf7GFP−TILもまた選択的にもっと多くの関連枯渇遺伝子を発現し、これらの遺伝子の発現が分化と関連していることを表明している。
メラノーマ患者の体内でTcf1+PD-1+CD8+ T細胞が存在している
その後、研究者はメラノーマ患者の外周血液CD8+ T細胞と原発性メラノーマを分析し、Tcf1+PD-1+CD8+細胞を確実に検出した。単細胞RNA-seqデータによると、人類メラノーマにTCF7+PDCD1+CD8A+ TILが含まれており、その遺伝子発現はマウスモデルで確認された細胞と似ている。TCGAデータベースの分析により、TCF7/PDCD1特徴は患者の生存率の改善に関連していると主張している。
研究者はこの研究がTcf1とPD-1を共発現する腫瘍内CD8+ T細胞が免疫治療において重要な役割を果たすことを示していると出張している。研究結果は免疫関与が抗腫瘍への免疫応答にどのように影響するかを理解するのに役立つ。これらの幹細胞様細胞の鑑定はすべての種類のガンの免疫治療をさらに改善すると期待できる。
参考文献
Intratumoral Tcf1+PD-1+CD8+ T Cells with Stem-like Properties Promote Tumor Control in Response to Vaccination and Checkpoint Blockade Immunotherapy
DOI: https://doi.org/10.1016/j.immuni.2018.12.021
サイヤジェン株式会社について
サイヤジェン株式会社は15年間の発展を経て、全世界の数万人の科学研究者にサービスを提供しており、製品と技術は直接にCNS (Cell、Nature、Science)の定期刊を含む5,200余りの学術論文に応用されています。弊社の「ノックアウトマウスライブラリ」は低価格だけでなく、遺伝子名称を入力すれば、ワンクリックで注文まで操作できます。 ノックアウトマウス、ノックインマウス、コンディショナルノックアウトマウス、トランスジェニックマウス、GFPマウス、免疫不全マウス、無菌マウスなどのカスタマイズサービスを提供する以外、専門的な手術疾患モデルチームがあり、多種の複雑な小動物手術疾患モデルも提供できます。
最新のプロモーション:
