-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
小児急性リンパ性白血病(ALL)は子供に最も多く見られる悪性腫瘍の一つ、現段階での中国の小児の治療率は約70%(国際最高の治療率は約80%)だ。治療薬に対する患者の耐薬性と再発が治療率を上げにくいボトルネックになる。そこで、小児白血病の耐性薬の再発とクローンの進化メカニズムをどのように解決するかがこの分野の研究の焦点となっている。
中国上海市交通大学医学部附属の上海市児童医学センター、国家児童医学センターの研究者は、「Blocking ATM—dependent NF-κB NF pathway overcomes niche protection and improves chemotherapy response in acute lymphoblastic leukemia」と題した記事を発表した。ALL細胞からのATM依存性を遮断する、NF-κBシグナル伝達は、骨髄微小環境対抗がん剤治療後の微小残留白血病細胞の保護効果を克服し、ALLの化学療法効果を画期的に高め、臨床後半期のALL連合治療に重要な意味を持つ。
この研究成果を発表し、血液学、伝染病学国際学術誌leukemia(《白血病》インパクトファクター(10.023)、論文の著者は、それぞれ中国の上海児童医学センターの小児科医学研究所所長周斌兵教授、上海の児童医学センターの小児科医学研究所の段才闻副研究員と上海の医学共同革新センターの主任陳紅専門教授である。

背景
リンパ性白血病(ALL)は子供に最も多く見られる悪性腫瘍の一つであり、主な子供の疾病で死亡する原因であり。リスク別の化学療法と改善支援治療では、ALL患者の5年間の生存率は80%以上だ。しかし、約20%の患者が再発し、治療に失敗する。したがって、ALL再発総合メカニズムの研究を行い、耐性とALLの再発を克服するための治療策を講じなければならない。
一連の研究では、突然変異が小児ALLの再発を引き起こすことを明らかにしている。科学者達は遺伝子分析と塩基配列解析によりいくつかの特定特異性の耐性薬の突然変異を特定すると同時に、残りの耐薬細胞は化学療法で生きられると主張した。その後、得られた耐性薬を使ったクローン進化を推進し、白血病は急速に増殖した。しかし、残りのALL細胞が抗がん剤治療の位置と生存メカニズムについては、まだ明らかになっていない。白血病細胞と微小環境(あるいは生態系)の間の相互作用は、再発の過程で重要な役割を果たしていることが明らかになった。
骨髓(BM)マイクロ环境は複雑かつうまく調整できるマイクロ环境で、造血幹細胞と細胞外基质と細胞因子からなる。造血の母細胞(HSCs)の安定的な状態を調節し、ALLの発症メカニズムと耐性も持つことになる。
重要な発見
中国の上海交通大学医学部附属の上海市児童医学センターの研究者は、抗がん剤疗法でALL細胞から分泌される細胞因子がBM細胞を集めて発達する環境を再構築し、残ったALL細胞を保護している。この細胞因子、すなわちGDF15, CCL3, CCL4は、ALLの展開において重要な役割を果たす。しかし、これらの細胞因子がどのように化学療法を通じて誘導されるかは未知である。
最新の研究では、研究チームが発見All細胞遺伝子療法による損傷回答(DDR)とNF-κBシグナル伝達の活性化、そのうちDDRカギ蛋白ATMと結合した汎化をつなぐ酵素の活性化TRAF6によるNF-κB核心な部分IκBを分解させ、NF-κB核心な部分P65蛋白を釈放し、核を促進し、その直接の下流细胞因子GDF15,CCL3とCCL4表現との分泌が増え、骨髄の中で形成残留白血病細胞の微小環境保護のため、残留白血病が再発して小さな細胞の生存を促進ALL耐薬が突発的に再発するための土台を作った。
これと共に、ATMとP65特異性小分子抑制剤で、ATM依存性を遮断するNF-κBシグナル伝達を利用し、共同臨床一線化薬物を使うことで、微細残留白血病の細胞を減らし、ALLの化学療法効果を高めることができる。
この研究の成果はオールの再発の前に複製の発生するメカニズムを解明し、ALL耐性の再発を克服する潜在的な治療的な点を明らかにした。
国際血液病専門家であるコロンビア大学癌遺伝研究所のAdolfo Ferrando教授は、今回の研究成果を高く評価し、「ALLの耐性が再発するのは世界的な悩みだ。ATM依存性を遮断するNF-κBシグナル伝達を利用しALL化効果は、臨床転換と治療の意味が大きいであり。
化学療法はALL細胞系と原代細胞の細胞因子の引き上げを引き起こす
研究者は以前、ALL保護環境が細胞因子(GDF15, CCL3, CCL4)によって再構築されていることを発見した。これらの細胞因子はCytrarabine (Ara−C)によって処理された後に調整される。
抗がん剤治療はこれらの細胞因子を誘導するメカニズムを決めるため、抗がん剤のカラーアールC、アグリセリン(DNR)、ケロピリン(MTX)、セミチン(VCR)、CTX、デキセミ(デックス)は、2つのALL細胞系(Nalm6、Reh)を治療した後、qRT−PCRで細胞の発現水準を測定した。
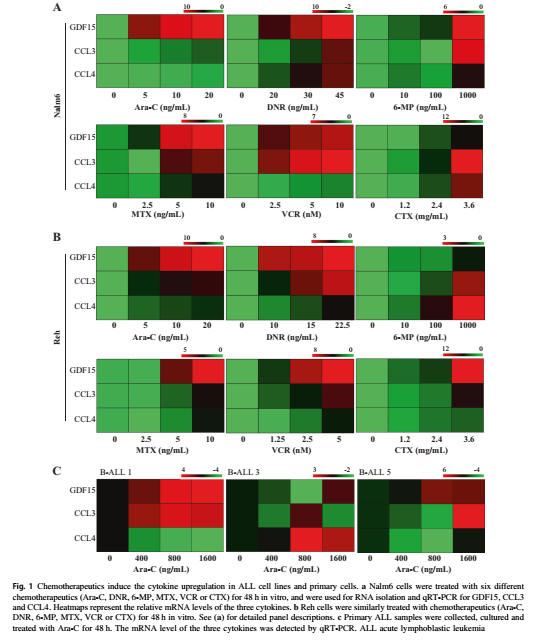
図に示されるように、Nalm6及びReh細胞におけるGDF15、CCL3及びCCL4のmRNAレベルは、薬物量の依存性が著しく増加する。実験ではさまざまな化学治療剤で、Ara-C、DNR、6−MPが、直接DNAの損傷や最も著しい細胞因子の上昇を引き起こし、研究に利用された。
研究者らは、mRNAのレベル検出を補完するため、Ara-C、DNR、6—MPなどで処理した後、ELISAでNalm6、Reh細胞の3つの細胞因子の分泌タンパク質のレベルを測定した。その結果、Nalm6及びReh細胞のうちの3つの細胞因子のタンパク質レベルが、散発的依存性の観点で著しく増加していることが示されている(図S1C及び図D)。このため、抗がん剤、特にDNA損傷剤は、BM微環境ではなく、ALL細胞のケモカインを直接誘導できると考えられる。抗がん剤疗法が行われるALL細胞系と原代細胞では、マイクロ环境保护に関する细胞因子の表现レベルが高くなっている。
化疗后NF-κB通路被激活
転写因子はNF-κBは、ストレス解消によってCXCL10とIL6のように細胞因子を調節することができ、腫瘍侵食と炎症反応に重要な役割をする。
本研究では、NF-βB経路が、マイクロ環境保護細胞因子の発現への関与を調節する可能性があることを明らかにした。彼らは、3aを経て、IキャパロBの蛋白質レベルが低下するという点を発見した(図3b)。これは、Nalm6とReh細胞の1つであるp65を、3b;(図S5A)。
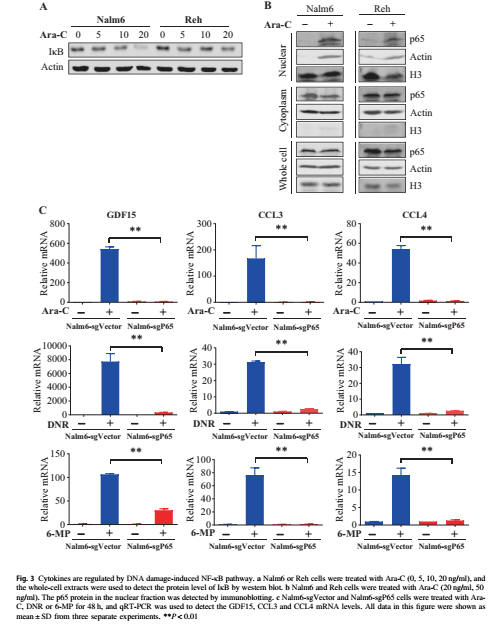
この結果、NF-κBシグナルは、Ara−Cを経て活性化された。NF-κBシグナルNと細胞因子アップの因果関係を研究するために、CRISPR/Cas9手段(Nalm6−sgP65とReh−sgP65)を用いてp65で低い細胞系を構築(図S5BとC)したところ、p65の細胞因子が、Ara−C、DNR、または6−MP処理によって著しく減少したことが明らかになった(図3c;(図S5D)。同様に、NF-κBシグナル阻害剤のPDTCが、細胞核の中に入ってp65をブロックし(図S5A)、Nalm6の細胞の中でAra−C処理を行って、細胞因子表現(図S5E)を抑制し、NF-κBシグナルの活性化と、体外調節GDF15、CCL3、CCL4の意思表示に参加する。
NF-κBシグナルは、ALL細胞に対する化学療法の感受性を高めた
研究チームはまたNalm6とReh ALLのマウスモデルで、ATM依存性NF-κBシグナル経由の化学的感受性を遮断するものと分析した。3回目の処理を経て、マウスを殺し、蛍光体蛍光共焦点撮影とFACにより頭蓋骨からGFP+ ALL細胞を検出する(図6 (a))。
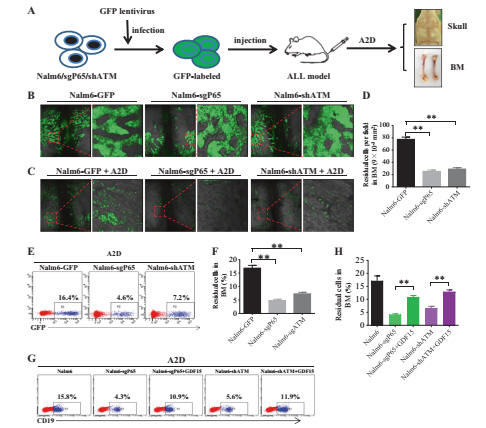
図6bに示すように、Nalm6-GFP、Nalm6-sgP65-GFP、及びNalm6-shATM-GFP細胞は、化学疗法の前に全ての血管を頭蓋骨の中に浸す。化学療法後Nalm6-sgP65-GFPとNalm6-shATM-GFPのマウスの頭の骨の中の残存GFP + ALLの細胞の数が著しくNalm6-GFPの子鼠(図6c, d)を下回っています。また10%を超えるGFP+ ALL細胞はNalm6−GFP子のBMに、5%未満のGFP+ ALL細胞はNalm6−sgP65−GFPとNalm6−shATM−GFP子(図6e, f)にとどまる。
その結果、体の中でATMへの依存性を示したNF-κBシグナルが活性化すると、Nalm6細胞のAra−Cに対する敏感性が高くなった。Reh ALL異種移植モデルでは、同様のデータが得られる(図s10a-e)。
GDF15は抗体をブロックすることで、ALL環境を抑制することができるため、外部ソースGDF15を追加することで、ATM依存性NF-κBシグナルを遮断する体の効果を逆転させることができると研究者は見ている。この仮説を検証するために、p65とATMは低ホール・モデルをクリックし、化学療法に敏感性がGDF15をソース性で追加することで逆転できるかを決定した。その結果、残留白血病細胞にGDF15が前処理された後、Ara−Cが処理するNalm6−shATMとNalm6−sgP65(図6g, h)が追加されていることが明らかになった。(サイヤジェンのノックアウトマウスを採用することになりました)
この研究の成果はALLの再発の前に複製の発生するメカニズムを解明し、ALLの耐性の再発を克服する潜在的な治療的な的点を明らかにした。
国際血液病専門家であるコロンビア大学癌遺伝研究所のAdolfo Ferrando教授は、今回の研究成果を高く評価し、「ALLの耐性が再発するのは世界的な悩みだ。ATM依存性を遮断するNF-κBシグナル伝達を利用しALL化効果は、臨床転換と治療の大きな意味であり。
リンク先:
Blocking ATM-dependent NF-κB pathway overcomes niche protection and improves chemotherapy response in acute lymphoblastic leukemia
https://www.nature.com/articles/s41375-019-0458-0
サイヤジェン株式会社について
サイヤジェン株式会社は15年間の発展を経て、全世界の数万人の科学研究者にサービスを提供しており、製品と技術は直接にCNS (Cell、Nature、Science)の定期刊を含む5,200余りの学術論文に応用されています。弊社の「ノックアウトマウスライブラリ」は低価格だけでなく、遺伝子名称を入力すれば、ワンクリックで注文まで操作できます。 ノックアウトマウス、ノックインマウス、コンディショナルノックアウトマウス、トランスジェニックマウス、GFPマウス、免疫不全マウス、無菌マウスなどのカスタマイズサービスを提供する以外、専門的な手術疾患モデルチームがあり、多種の複雑な小動物手術疾患モデルも提供できます。
最新のプロモーション:
