-
サイヤジェンニュースお申し込み サブスクライブすると、研究動向とキャンペーンを取得いただけます。
-
お問合せフォーム
高齢化は、世界の現在及び将来における最も重要な社会問題の1つであり、人類寿命の伸長と先進国の出産率の持続的な低下に伴い、2050年までに世界で21億人の年齢が65歳を超え、そして2100年になると、この数字は31億人に達する見込みである。
一方では、高齢化が労働力の損失を齎すが、もう一方では、社会的医療コストの急激な上昇を引き起こす。この様な現象が起きる原因は主に高齢者多発性疾患と関係している。神経変性疾患は、年齢と共に幾何級数的に発病率が増加される一種の疾患である。現在すべての神経変性疾患において、対応できる特効薬や治療法などがまだなく、例え病気の進行を遅らせる医薬品でも非常に少ないので、今のところ唯一の方法は、良好な生活習慣を通じて罹患率を低下させ、且つ、発症時間を遅延させることである。
神経変性疾患の患者の死後の剖検では基本的に脳萎縮現象がみられるが、これはニューロンの死亡と樹状軸の突起減少と密接な関係があり、今は無数の科学研究者と大量の経費がこれらの疾患の研究及び薬物の開発に投入されている。サイヤジェン株式会社は、長年生物学分野に深く取り組んでいるので、神経疾患特には神経変性疾患方面の研究で豊富な経験を積んだ。当該ガイドブックは、科学研究の観点から一般的な神経変性疾患の典型的な研究手法の説明を趣旨としている。我々はこれらの典型的な研究手法に基づいて、便利なワンストップ式科学研究サービスをお客様に提供する。
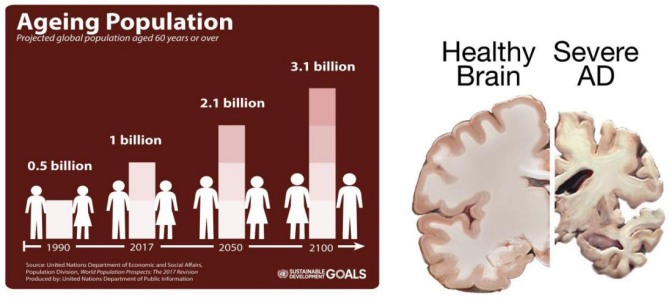
図1. 高齢化及び神経変性疾患の主な特徴
神経変性疾患はその後期で中枢神経系全体に損傷を与え、患者の死亡をもたらす。しかし発病の過程で、彼らの攻撃対象はまだ少し異なる。
(1)アルツハイマー病(Alzheimer Disease,AD):アルツハイマー病の初期の主要な病巣は一般的に海馬と前頭側頭葉の錐体ニューロンから発生し、記憶喪失の症状を表現して、最近の出来事をすぐ忘れがちである。これと同時に集中困難であり、ひいては数分前の対話内容さえ忘れてしまう。
(2)パーキンソン病(Parkinson Disease, PD):パーキンソン病とは、中脳の黒質部でドーパミンを放出するニューロンの損傷を受け、次いでその投射領域(主に線条体)の運動抑制機能が無効になり、患者には非自主的震え及び運動制御能力の衰退が発症する。
(3)筋萎縮性側索硬化症(Amyotrophic Lateral Sclerosis, ALS):筋萎縮性側索硬化症では運動皮質或は末梢運動神経が損傷を受け、殆どの患者は診断後すぐに運動能力を全面喪失し、呼吸影響にまで至り、最終には死亡する。
(4)ハンチントン病(Huntington Disease, HD):ハンチントン病患者は、線条体のニューロンが死亡し、自己行動や感情の制御力が弱くなり、認知機能や運動機能が著しく損傷される。
(5)前頭側頭葉認知症(Frontotemporal Dementia, FTD):前頭側頭葉認知症とレビー小体型認知症(Dementia with Lewy bodies, BD)は、認知記憶の障害を主とする。プリオン病(Prion Diseases)は、タンパク質の変化を内因とする神経障害(ニューロパチー)である。
(6)多発性硬化症Multiple sclerosis(MS):多発性硬化症は、軸索外側の髄鞘組織に狙いをつけて、髄鞘は、自己免疫系の攻撃を受け、神経の電気信号の伝達を遅らせて弱化し、患者の動きと呼吸に影響を与える。
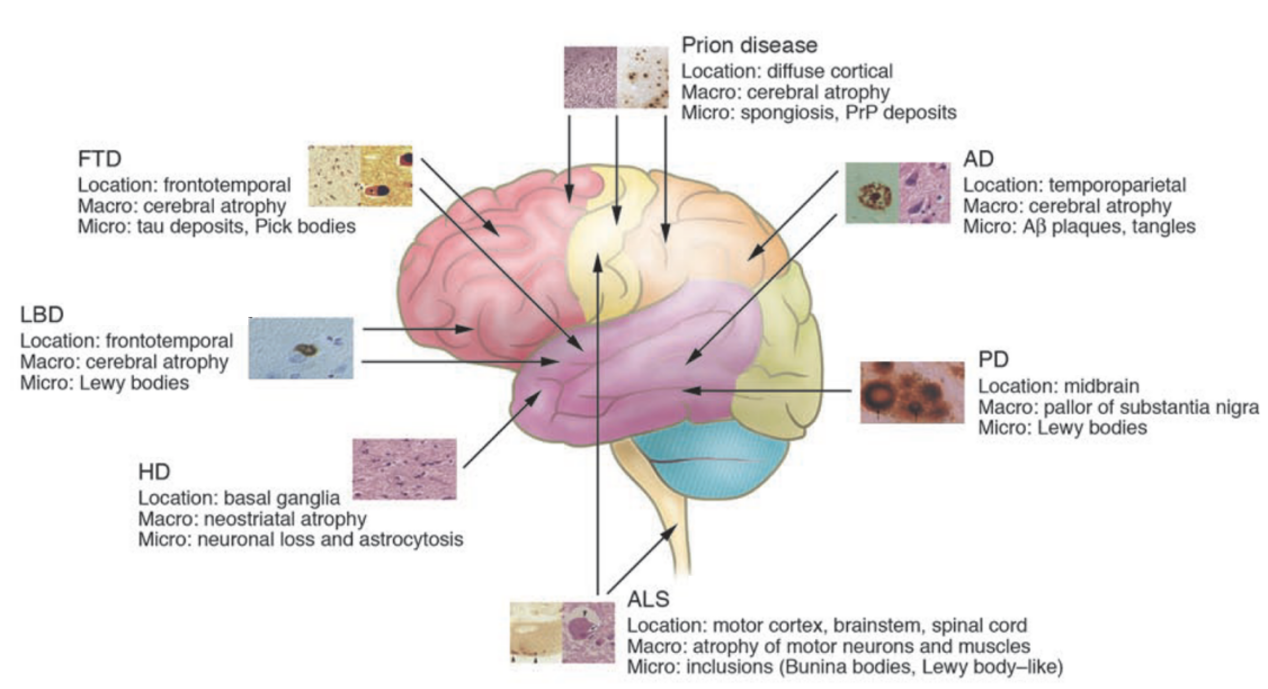
図2. 主な神経変性疾患の病変と病理の概要説明
(Source: 10.1172/jci24761)
主な神経変性疾患の罹病率
図2に示す疾患の中で、ADの罹病率が最も高く、10万人あたり約1200人が病気にかかっており、もし65歳以上の高齢者に絞った場合、その発病率は10%を超える。発病率第2位はPDであり、全年齢層での発病率は約0.3%である。
次からはその患者比例は多くはないが、しかし絶対無視できないFTD、HD、ALSである。HDとFTDの発生率に明らかな性別差はなく、その中のHDは唯一の病原性遺伝子が確定された疾患である。PDとALSは男性のよくかかる病気であり、その男性患者数は女性患者のほぼ2倍であるが、ADはその逆であり、女性患者は男性患者の約1.4倍ぐらいである。遺伝的観点から考察すると、HDは100%優性遺伝性疾患である以外で、ADやPDなどの一般的な神経変性疾患は主に散発的な症例である。
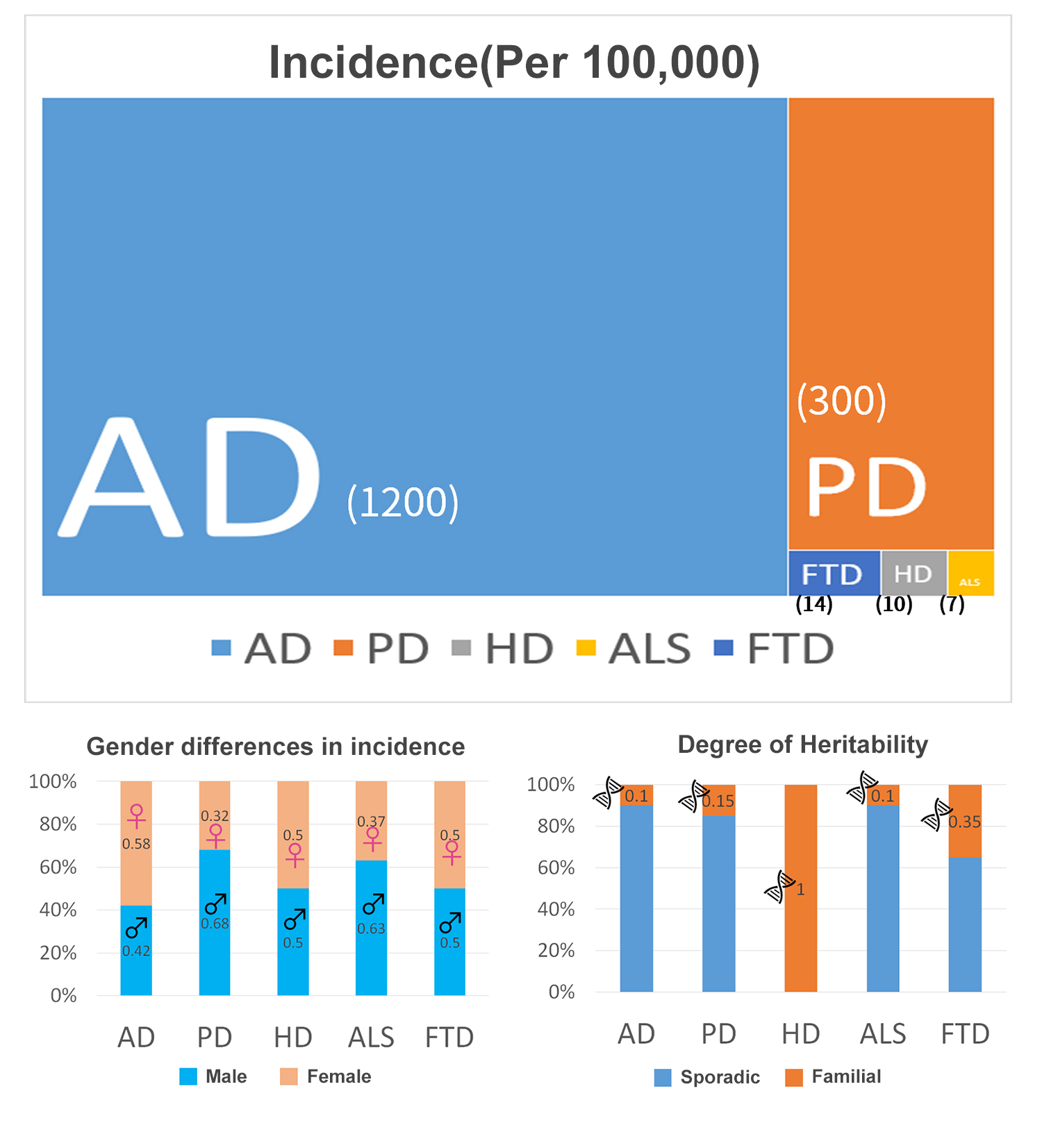
図3. 神経変性疾患の疫学的特徴
1.良くある神経変性疾患とそのモデル
如何なる病気の研究であっても、動物モデルは必要不可欠で、神経変性疾患もその例外ではない。従って、この類の研究の第一歩は、適切な動物モデルの選択或は作製である。現在ラットやマウスを代表とするげっ歯類モデルがあり、神経変性疾患の研究の主力となっており、異なる疾患は、その病理学的特徴が異なる為、その標的とする目標遺伝子も異なくなる。以下はいくつかの主な神経変性疾患モデルである。
- アルツハイマー病(AD):殆どのADモデルは、Aβ前駆体とスプライシング酵素(PS1/2)及びtauへの遺伝子編集を通じて作成される。この他に、大脳局在を通じてこの二種類の毒性タンパク質を注射する急性モデリングもある。また、APOEはADと関与しているが、その自体をADモデルとして使用できず、従来のADモデルと交配して研究する必要である。BACE1もAβの形成に関与しているが、今現在人体で変異によりAD形成できたとの報告はまだない。他にもTREM2を代表とする免疫関連遺伝子があるが、APOEと同様に、これらの遺伝子編集の動物はまだ単独でADの動物モデルとして扱うことはできない。
- パーキンソン病(PD):PDの場合、α-Synucleinはニューロンのレビー小体を構成する主成分であり、勿論PD動物モデルを構築する為の主力遺伝子である。ただAD研究におけるAPPとそのスプライシング酵素遺伝子の支配的位置とは異なり、家族性PD研究におけるPINK1、Parkin、LRRK2とDJ-1などの遺伝子も非常に大きな割合を占めており、これらの遺伝子の殆どはα-Synucleinの集合を抑制してその分解を促進する過程で役割を発揮する。しかし、全体的に言うと、PD遺伝子編集のモデル表現型はAD疾患の表現型ほど明確ではないため、従って、しばしばMPTP、Roteona、6-OHDAなどの薬剤を使用してPDモデルを構築する。
- ハンチントン病(HD):HDは、モデリング為の一番簡単な疾患である。なぜかというと、この病気はHttタンパク質の中でCAGリピート数が多すぎることが原因となっている為、モデリングがすべてHtt遺伝子を対象とするが、ただ遺伝子編集の方法とCAGリピート数に少し差があることである。
- 筋萎縮性側索硬化症(ALS):筋萎縮性側索硬化症に関わる遺伝子は比較的に多くまた複雑で、あるものは常染色体上にあり、あるものは性染色体上にある。優性疾患もあれば、劣性疾患もあることから、モデルも多様であり、最も早く発見されたのはSOD1であり、最近の10年間の研究で比較的に多かったのはタンパク質凝集体を形成するTDP-43と散発性ALSの中で最もよく見られるC9ORF72である。
- 前頭側頭葉認知症(FTD):当病気はADと同様にタウの集積があり、またALSの特定的タンパク質TDP-43にも関連してあるが、ただしALSとの関与が一番深く、多くのタンパク質変異はALSの誘因でもあるし、同時にFTDも誘発するが、興味深いのは、これら2つの病気の一つは運動能力の損傷をメインとし、もう一つは主に認知能力を損傷させる。
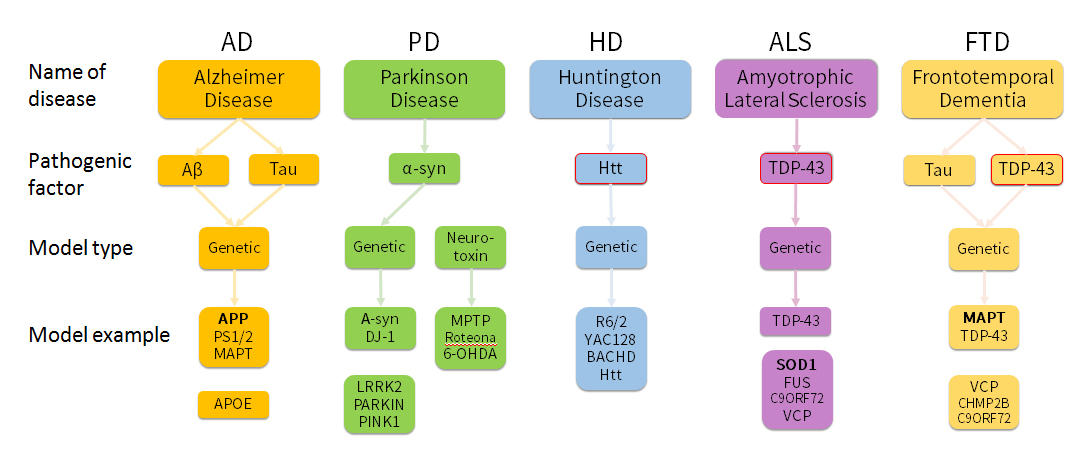
図4.一般的神経変性疾患の主な病原性遺伝子及びそのモデル
(Source: 10.1016/B978-0-12-809468-6.00042-5)
2.遺伝子編集と疾患動物モデル
倫理上の問題から、人間から組織サンプルを採取して神経変性疾患の研究を行うことは困難である。従ってマカク、マーモセット、ラット、マウス、ゼブラフィッシュ、ミバエと線虫などのモデル動物が開発されている。霊長類が人間に更に近く、医学研究モデルとして理論上にも一番理想的であるが、コストが高すぎることに加えて、実験サイクルが長く、遺伝子編集が困難である。ゼブラフィッシュとショウジョウバエは、ハイスループット研究に一層適しており、繁殖速度が速くて実験コストも比較的に低いが、認知機能に関連する多くの表現型研究では、その神経系が余分に単純である為、実施不可能である。要約すると、げっ歯類動物と人間は遺伝子的に90%以上類似しており、その上に実験サイクルが霊長類よりもはるかに短く、人間の認知プロセスが基本的にそれらの身の上で再現でき、更に大量な研究データの蓄積と比較的低いコストなどがあるから、現在最も理想的な動物モデルと見なされている。
2009年から2013年の間に様々なヌクレアーゼ技術の爆発的な発展とその後の継続的な改善に伴い、特にCRISPR / Cas9技術の発明により、遺伝子編集の効率が大幅に向上し、難度とコストも大幅に低くなるので、神経変性疾患の研究で重要な役割を果たしている。
遺伝子組み換えは遺伝子編集で先に登場し、今も最も多くの疾患モデルを持っている遺伝子操作法でもあるが、移入された遺伝子のコピー数の不確定、挿入部位の不確定、過剰発現しかできないなど欠点がある。従って、遺伝子発現をより制御可能にし、且つ、ランダムな挿入による他の遺伝子発現に影響を与えないようにするために、この方法を、徐々に他の方法に代替してゆく。
遺伝子発現を増加させる遺伝子組み換えの過剰発現とは異なり、遺伝子発現を減少または排除する必要もあるため、遺伝子ノックアウト技術が誕生した。この方法は遺伝子全体またはエキソンを直接ノックアウトするか、或いはフレームシフト変異を引き起こしてこの遺伝子産物の転写の活性を喪失させるか或は機能を完全に失うようにする。マウスの遺伝子の30%は完全にノックアウトされて死亡していることが報告されている。そのため一方では胚胎の致死を回避し、他方ではより精細な研究を目指し、Cre-LoxP法が誕生され、この方法はCreの連結前のプロモーターに基づいてCreの切断酵素の発現時間と発現位置を決定し、ノックアウトされる標的遺伝子の両側にloxp部位を連結するだけで済む。
Cre-LoxP法を少し改善して遺伝子ノックインに利用でき、その一方では、両端に持つLoxPの終結配列と外来遺伝子のフラグメントをマウスゲノムに挿入し、繁殖用マウスはCreマウスと交配後に外来遺伝子の終結配列がノックアウトされた後にのみ発現できる。
補償やイントロンの影響により、単一又は複数の遺伝子の変化では明確な表現型を生成することができず、また染色体への大きなセグメントのノックアウトやコピーなどの操作も実行でき、これらの変化は多くの遺伝病でもよく発生する。
動物実験の目的は、人間への応用であるため、上記の遺伝子編集方法に基づいてまたキメラマウスが誕生して、この種のマウスは異なるマウスの細胞を同時に持つこともでき、更に、人間とマウスの細胞を両方とも持つことができるが、しかし人間の細胞を加入するには倫理的な問題がある。
現在一番流行しているモデル構築方法は、ヒト化である。この方法はマウスにヒト遺伝子を導入し、必要に応じて元の遺伝子を代替するかしないかを選択でき、イントロンを必要とするかどうかを選択できるが、単一の遺伝子は依然として大きなセグメントの染色体断片である。
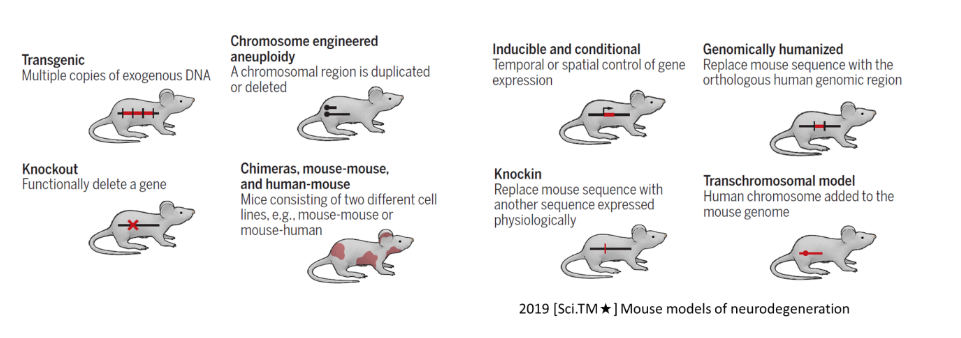
図5. 神経分野における一般的タイプの遺伝子編集マウス
(Source: 10.1126/scitranslmed.aaq1818)
研究の進展につれ、多くの伝統的な遺伝子組み換えモデルはもはや科学研究の革新要求を満たすことができなくなった。従って、新しい遺伝子と神経変性疾患との関係を研究し、正確な(時間と空間上)治療薬の疾患への治療効果を研究する際に薬物処理やウイルス注射などと必然的に関与する必要がある。多くの科学研究者たちの精力と時間を節約する為に、サイヤジェン株式会社の神経科学におけるワンストップソリューションは、革新的な遺伝子編集モデルと疾患モデルとの交配繁殖、プラスミド構築、ウイルスパッケージング、神経幹細胞遺伝子編集、外因性ウイルス薬の定位脳注射、組織病理学的蛍光イメージング及び無菌マウス脳腸軸など技術的作業でお手伝えできれば幸いである。実験技術を学ぶのではなく、ワンストップサービスの体験を楽しみにし、科学問題の解決に注意力を集中させる狙いである。
3.神経変性疾患におけるマウスとヒトの年齢の関係
神経変性疾患は自閉症、精神分裂症など青春期または成人期になったばかりの時に症状を起こす他の精神疾患と比べ、発症時期が比較的に遅く、殆どの患者は50歳以降に発症し(よく知られている神経変性疾患の中でもハンチントン病と多発性硬化症の発症は早い。従って相応なる実験ウィンドウも比較的に後回しされているが、現在は遺伝子編集でこれらのマウス疾患モデルの発症時期を早ませることも可能で、ヒトの発症時期との対応関係をそれほど厳密でなくなる為、マウスの研究結果を慎重に扱う必要があり、完全にそのままで人体実験で踏襲することはできない。しかし、そうだとしても、動物実験は人体実験の前哨基地として、莫大な貢献と役割を果たしている。
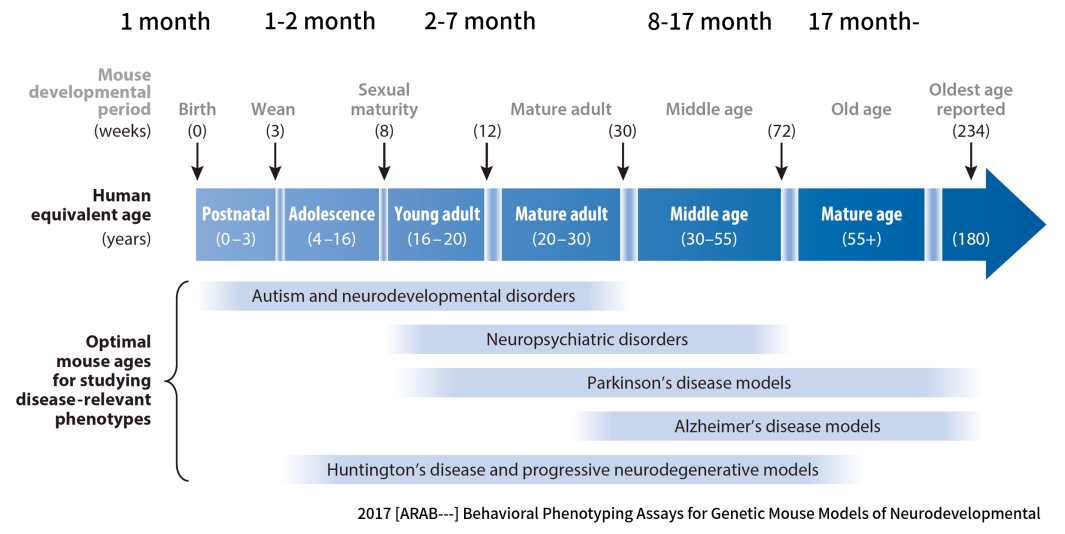
図6.神経変性疾患におけるマウスとヒトの年齢関係
(Source: 10.1146/annurev-animal-022516-022754)
神経変性疾患の発症時期について、我々はマウスを様々な疾患に適した年齢にまで育てて実験を行う必要があり、例えばパーキンソン病のマウスでの殆どの実験は10週間から60週間の間に行う必要があるが、アルツハイマー病の研究時期は大体20週間後である。遺伝子組み換えと遺伝子編集されたマウスはその遺伝子改変を施し、その繁殖力、表現型等全部異なる程度の影響を受ける可能性があり、マウスの繁殖および飼育に新たな要求を必要されている。
サイヤジェン株式会社のモデル動物研究センターは、江蘇省太倉市(上海近郊)、広州科学都市の中心部と河北省固安(北京近郊)等に合計40,000平方メートルの新しい動物施設を持っており、25,000平方メートル以上のSPF級動物実験室を持ち、1,600セット以上のIVC飼育設備を備え、SPFレベルのラットとマウスを15万ケージ以上繁殖でき、動物の個体数規模は50万を超える。そしてその健康検測、遺伝子管理から人材トレーニング、個別化繁殖などまで、動物の飼育と繁殖の要件を全面的に満足できる。F1世代のマウスを入手して自己繁殖も可能だが、サイヤジェン株式会社によって専門的かつ効率的に増殖でき、十分な数の実験用マウスを迅速に入手できる。増殖後のマウスはサイヤジェン株式会社で代わって適合な年齢にまで飼育も可能である。また必要に応じてマウスを取り戻して独自の実験を行うか或はサイヤジェン株式会社の技術サービスプラットフォームで続きの実験を継続したりすることもできる。
4.神経科学研究で最も一般的に使用される表現型分析法
三大神経生物学ジャーナル(Neuron、Nature Neuroscience、Journal of Neuroscience)に過去5年間に掲載された研究論文の数の統計を行った。モデルの選択の方面で、ラット、マウス、神経幹細胞が50%以上を占めているが、ほか細胞系や非ヒト霊長類などは半分未満である。
その中でマウスは遺伝子編集関連のモデル分野で最も高い割合を占めており、ラットはより発達し、より簡単にトレーニングできる特性などから神経変性疾患の研究において重要な位置を占めている。ほかには、ラットおよびマウスをモデルとして扱っている上記の文献の中では、動物モデルを応用した研究のなかで、免疫蛍光組織化学、行動学およびウイルスのトランスフェクション/追跡などの方法が特に重要視されている。
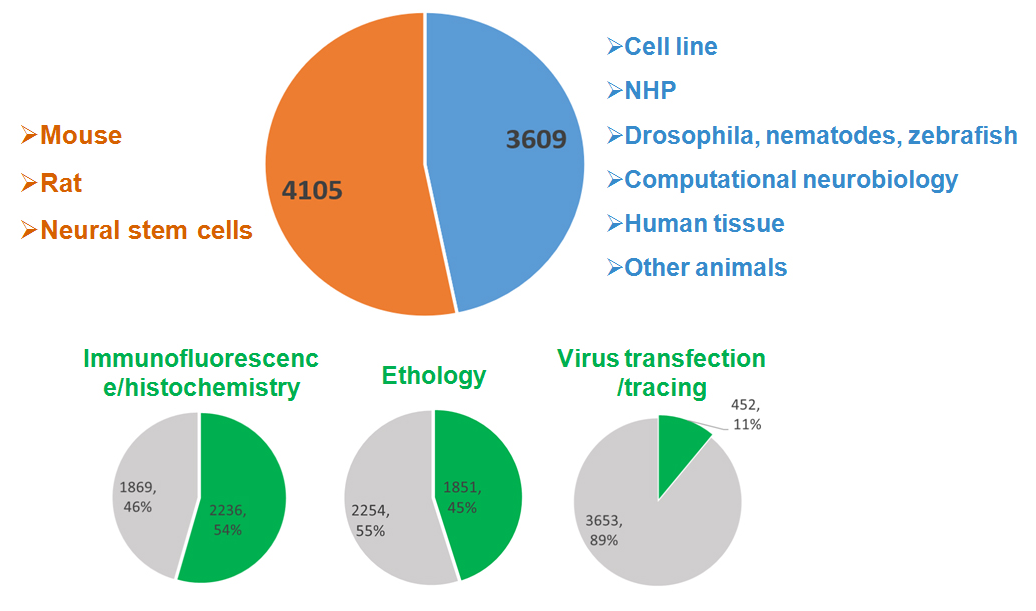
図7. 三大神経生物学ジャーナルにおける過去5年間発表論文の分析
サイヤジェン株式会社の成熟且つ安定した革新的な医薬品研究開発プラットフォームは神経科学研究のための様々な行動学、免疫蛍光組織化学技術サービスの提供が可能であり、また、プラスミドウイルスベクターを代わりで設計して、迅速に特定の脳領域ベクター注射を可能とし、後期の病理学的検証と組み合わせ、すぐに貴重なデータを取得できる。
神経変性疾患における動物の行動研究は大体学習と記憶、運動バランス、感情的精神、社会的コミュニケーションの四つのパーツに分ける。一般的な神経変性疾患は後期になるとこれらの方面で深刻な影響があるが、様々な疾患が影響する主な方向は異なり、図表のなかで三つの最もよく知られている神経変性疾患の通常の行動学研究方法をまとめた。
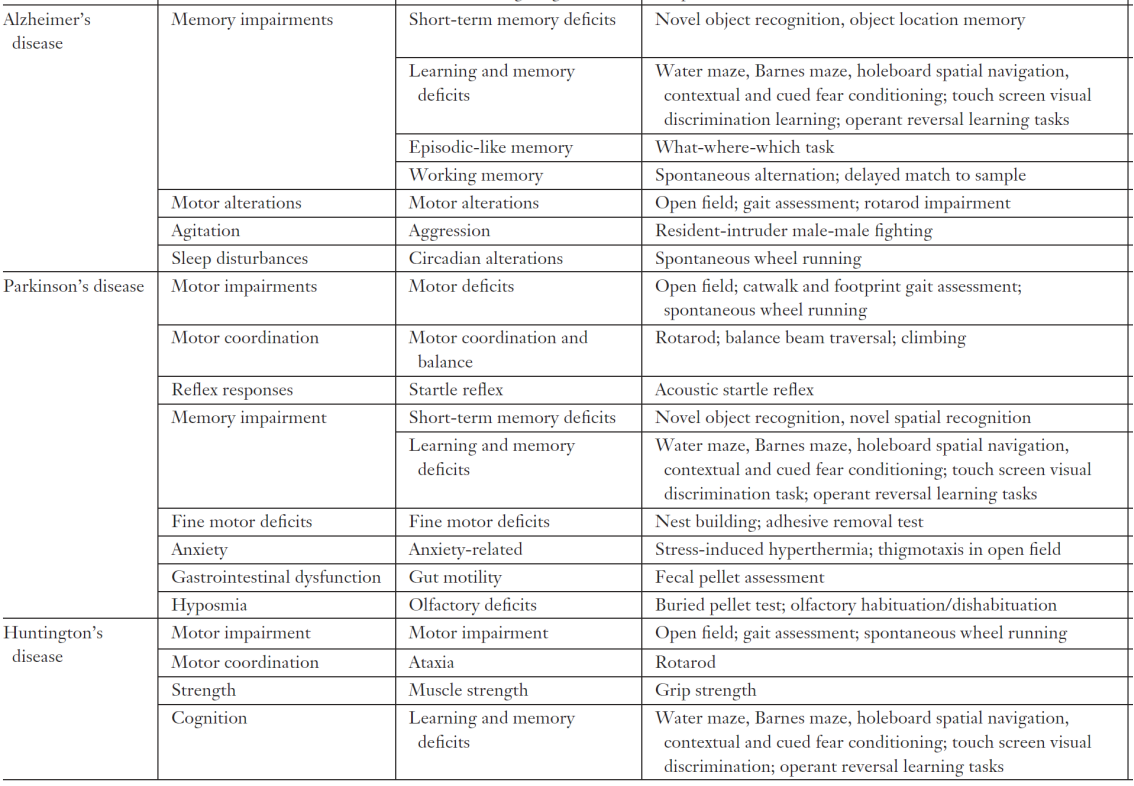
表1. げっ歯類で一般的に使用される行動実験方法
サイヤジェン株式会社の小動物表現型分析プラットフォームは様々な行動実験サービスを提供できる。サイヤジェン株式会社のプラットフォーム施設で独自の実験ができ(動物操作ライセンスとプラットフォームトレーニングが必要)、サイヤジェン株式会社の小動物表現型分析プラットフォームの技術者に実験を委託することも可能である。現在、サイヤジェン株式会社が提供する行動実験プロジェクトには次のものを含む。
- 学習記憶能力検出:水迷路、Barnes迷路、放射状迷路、新しい物体認識、T / Y迷路など。
- 運動能力検出:Rotarod、歩行姿勢計、テールサスペンション試験機など。
- 情緒検出:野外実験、強制水泳、高架式迷路、砂糖水の好みなど。
ボディ、器官、細胞及び分子レベルの四つのステップで動物行動評価システムの基準と方法の研究をサポートできる。
標的または標的タンパク質が確定された場合、神経変性疾患の一般的な実験手順は次のとおりである:
1.興味のある遺伝子編集動物をカスタマイズできる:この種の作業は時間と手間がかかり、普段は専門会社に委託できる。もし動物を薬力研究或は表現型の研究に使用する場合には更なる強化が必要であり、薬物補助またはウイルス注射の方式で動物を処理する必要がある。
2.行動実験による疾患の表現型または薬効の検証:メカニズム実験では組織切片を介した同所への病理学的検出、またはアポトーシスと老化の検出、および従来の分子及びタンパク質シグナル伝達経路因子の発現と修飾に関する研究が必要である。
3.電気生理学的実験:電気生理学的実験も一種の表現型検証であり、光遺伝学、およびカルシウムイメージング技術の現在の発展で部分的に電気信号の入力及び出力機能を代替できた。もちろん、これは電気生理学が重要ではないという意味ではなく、一部のみ他の方法で置き換えできるという意味合いである。
15年間の発展を経て、サイヤジェン株式会社の成熟で安定した革新的な薬物研究開発プラットフォームは、沢山の神経科学研究者様のために何千例もの遺伝子ノックアウトベクター、遺伝子ノックアウト細胞モデル、遺伝子ノックアウトラットおよびマウスモデルを構築し、モデルのカスタマイズ、ベクターパッケージング注入、行動実験、病理学的マーカー検出、およびメカニズム探索のワンストップサービスの提供に努めてきました。関連記事はNeuron、Nature Neuroscience、Journal of Neuroscienceなどの神経生物学専門ジャーナルに掲載されています。
References:
1.Lars Bertram, Rudolph E. Tanzi. The genetic epidemiology of neurodegenerative disease.
J Clin Invest. 2005;115(6):1449-1457. https://doi.org/10.1172/JCI24761.
2.Aline S. de Miranda, Roberto Andreatini, Antônio L. Teixeira. Chapter 43 - Animal Models of Mania: Essential Tools to Better Understand Bipolar Disorder, Editor(s): P. Michael Conn,
Animal Models for the Study of Human Disease (Second Edition), Academic Press, 2017,
Pages 1131-1143, ISBN 9780128094686, https://doi.org/10.1016/B978-0-12-809468-6.00043-7.
3.Elizabeth M. C. Fisher, David M. Bannerman. Science Translational Medicine 22 May 2019: Vol. 11, Issue 493, eaaq1818. DOI: 10.1126/scitranslmed.aaq1818
サイヤジェン株式会社について
サイヤジェン株式会社は15年間の発展を経て、全世界の数万人の科学研究者にサービスを提供しており、製品と技術は直接にCNS (Cell、Nature、Science)の定期刊を含む5,200余りの学術論文に応用されています。弊社の「ノックアウトマウスライブラリ」は低価格だけでなく、遺伝子名称を入力すれば、ワンクリックで注文まで操作できます。 ノックアウトマウス、ノックインマウス、コンディショナルノックアウトマウス、トランスジェニックマウス、GFPマウス、免疫不全マウス、無菌マウスなどのカスタマイズサービスを提供する以外、専門的な手術疾患モデルチームがあり、多種の複雑な小動物手術疾患モデルも提供できます。
